
| A��Ư����Һ�ڿ�����ʧЧ��ClO����CO2��H2O��HClO��HCO3�� |
| B����FeCl3��Һ��ʴͭ����ӡˢ��·�壺Fe3����2Cu��Fe2����2Cu2�� |
| C����NaAlO2��Һ��ͨ�����CO2��Al(OH)3��AlO2����CO2��2H2O��HCO3����Al(OH)3�� |
| D��̼�������Һ�м����������������Һ��HCO3����OH����CO32����H2O |


 ���100�ֵ�Ԫ�Ż�������ϵ�д�
���100�ֵ�Ԫ�Ż�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��Na2O2��H2O��Ӧ:2 +2H2O +2H2O 4OH-+O2�� 4OH-+O2�� |
B��FeCl2��Һ��ϡ���ᷴӦ:Fe2++N +4H+ +4H+ Fe3++NO��+2H2O Fe3++NO��+2H2O |
C��CaCO3�������Һ��Ӧ:CaCO3+2H+ Ca2++CO2��+H2O Ca2++CO2��+H2O |
D��KAl(SO4)2��Һ�백ˮ��Ӧ:Al3++3NH3��H2O Al(OH)3��+3N Al(OH)3��+3N |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ѡ�� | ��ѧ��Ӧ�������ӷ���ʽ | ���� |
| A | Fe3O4��ϡ���ᷴӦ��2Fe3O4+18H+ =6Fe3++H2��+8H2O | ��ȷ |
| B | ��̼��þ�м���ϡ��� +2H+ =CO2��+H2O +2H+ =CO2��+H2O | ����̼��þ��Ӧд��������ʽ |
| C | ���������Һ�м�������������Һ�� Ba2++  =" " BaSO4�� =" " BaSO4�� | ��ȷ |
| D | FeBr2��Һ������ʵ�����Cl2��Ӧ�� 2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 | ����Fe2+��Br-�Ļ�ѧ������֮��ӦΪ1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
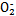 �������۳�ȥ����֪�˷�Ӧ��ϵ�к���Al��NaAlO2��NaNO2��NaOH��NH3��H2O��H2O�������ʡ�
�������۳�ȥ����֪�˷�Ӧ��ϵ�к���Al��NaAlO2��NaNO2��NaOH��NH3��H2O��H2O�������ʡ�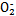 �������س�ȥ������
�������س�ȥ������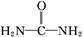 )��N
)��N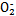 �����������·�Ӧ�������������塣�÷�Ӧ������16.8 L(������Ϊ��״��)�������ʱ,�������ص�����Ϊ�������� g��
�����������·�Ӧ�������������塣�÷�Ӧ������16.8 L(������Ϊ��״��)�������ʱ,�������ص�����Ϊ�������� g�� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ữ�ĺ����ҽ���Һ����ȡ�⣺2I����H2O2=I2��2OH�� |
| B������ʹ�������������Һ��ɫ��2MnO4��+5C2O42��+16H+=2Mn2++10CO2��+8H2O |
| C�������������Һ��ϣ�2H����Cl����ClO��=Cl2����H2O |
| D������������Һ�е�������������Һ��pH=7��Ba2++OH��+H++SO42��=BaSO4��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������þ��ɫ���������Ȼ����Һ��Mg(OH)2��2NH4+��Mg2+��2NH3��H2O |
B��ͭƬ�ӵ�Դ������̼,���ӵ�Դ���������������ҺCu��2H�� Cu2����H2�� Cu2����H2�� |
C������һ������Һˮ�⣺HPO42����H2O PO43����H3O�� PO43����H3O�� |
| D��Ư����Һ�м��Ȼ�����Һ�����������ɫ������ Fe3+��3ClO����3H2O��Fe(OH)3����3HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A������������������ |
B����ˮ��ͨ������������ |
C��̼��������Һ�м������ |
D��������Һ�м������ ��Һ�� ��Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������Լ��Ե�ԭ��CO32��+ 2 H2O = H2CO3 + 2 OH�� |
B��ϡ�����ϡ����������Һ��Ӧ���к��ȡ�H=��57.3 kJ/mol����ϡ������ϡ����������Һ������Ӧ���Ȼ�ѧ����ʽ��ʾΪ��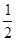 H2SO4(l)+ KOH(l) = H2SO4(l)+ KOH(l) = 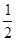 K2SO4 (l)+ H2O(l) ��H=��57.3 kJ/mol K2SO4 (l)+ H2O(l) ��H=��57.3 kJ/mol |
| C��������Һ�еμ�����������Һ�����������ʵ������ 2 Al3+ +3 SO42��+3 Ba2+ +6 OH�� =" 2" Al(OH)3 ��+ 3 BaSO4 �� |
D��ͭ��Ũ�����ϼ��ȣ�2H2SO4��Ũ��+Cu SO2��+Cu2+ +SO42��+2 H2O SO2��+Cu2+ +SO42��+2 H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com