
(12分)在右图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C,D为夹在滤纸两端的铂夹,X,Y分别为直流电源的两极。在A,B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入铂电极。切断电源开关S1,闭合开关S2,通直流电一段时间后

请回答下列问题:
(1)标出电源的正、负极:X为___极,Y为___极。
(2)在滤纸的C端附近,观察到的现象是_ ___,在滤纸的D端附近,观察到的现象是__ __。
(3)写出电极反应式:A中_ ___;B中_ ___;C中__ __;D中_ ___。
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2,闭合开关S1,则电流计的指针是否发生偏转(填“偏转”或“不偏转”)__ __。[来源:ZXXK]
(5)若电流计指针偏转,写出有关的电极反应式(若指针“不偏转”,此题不必回答):
A中___ __ __ __ __ _;B中__ __ __ ____ __。
若电流计指针不偏转,请说明理由(若指针“偏转”,此题不必回答)__ __ __ ___ _ ____ __ __ _ ____ _ __ __ _ __ __。
(1)正极;为负极 (2)试纸变蓝 ;试纸变红
(3)4H++4e-=2H2↑;4OH--4e-=2H2O+O2↑;4I--4e-=2I2;4H++4e-=2H2↑。
(4)偏转 (5)2H2+4OH--4e-=4H2O ;2H2O+O2+4e-=4OH-
【解析】该试题在知识网络交汇点设计的试题,强调了学科的内在联系和知识的综合,这有利于发挥高考对促进素质教育的导向功能。本题就是在电化学知识网络交汇点——电解池与原电池的结合与互换上命题,符合高考命题思路,体现了考试说明的要求。所以在化学学习的过程,更应注重学科内的知识的内在联系,构建知识网络,培养学生学科能力。
(1)电解KOH溶液实际就是电解水,所得产物为H2和O2,因为A试管中气体体积是B试管的2倍,所以A中为H2,B中为O2,即A为阴极,B为阳极,所以X为正极,Y为负极。
(2)C与电源正极相连,为阳极: 2I--2e-=I2,故试纸变蓝。
D与电源负极相连,为阴极:2H++2e-=H2↑,故试纸变红。
(3)A是阴极,氢离子放电,电极反应式是4H++4e-=2H2↑;B是阳极,OH-放电,电极反应式是4OH--4e-=2H2O+O2↑;C是阳极,I-放电,电极反应式是4I--4e-=2I2; D是阴极,氢离子放电,电极反应式是4H++4e-=2H2↑。
(4)如果切断S2,闭合S1,则可由A中的H2,B中的O2与KOH溶液形成H2,O2燃料电池,把化学能变为电能,故指针偏转。
(5)在原电池中负极失去电子,发生氧化反应。正极得到电子,发生还原反应。所以A极电极反应式是2H2+4OH--4e-=4H2O ,B极极反应式是2H2O+O2+4e-=4OH-


科目:高中化学 来源:2012-2013学年河南省扶沟高中高二上学期第一次考试化学试卷(带解析) 题型:填空题
(12分)在右图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C,D为夹在滤纸两端的铂夹,X,Y分别为直流电源的两极。在A,B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入铂电极。切断电源开关S1,闭合开关S2,通直流电一段时间后
请回答下列问题:
(1)标出电源的正、负极:X为___极,Y为___极。
(2)在滤纸的C端附近,观察到的现象是_ ___,在滤纸的D端附近,观察到的现象是__ __。
(3)写出电极反应式:A中_ ___;B中_ ___;C中__ __;D中_ ___。
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2,闭合开关S1,则电流计的指针是否发生偏转(填“偏转”或“不偏转”)__ __。[来源:学科网ZXXK]
(5)若电流计指针偏转,写出有关的电极反应式(若指针“不偏转”,此题不必回答):
A中_____ ____ __ _;B中__ ________ __。
若电流计指针不偏转,请说明理由(若指针“偏转”,此题不必回答)____ __ ___ _ ____ __ __ _____ _ __ __ _ __ __。
查看答案和解析>>
科目:高中化学 来源:2013届江苏省苏南四校高三12月月考试化学试卷(带解析) 题型:填空题
(12分)双氧水、过硫酸钾是工业上常用的氧化剂、消毒剂。工业上以铂为阳极,铅或石墨为阴极,电解NH4HSO4溶液得过硫酸铵【(NH4)2S2O8】溶液,其工艺流程为:
(1)将电解后的溶液送往水解器中在减压条件下水解、蒸馏、浓缩分离,精馏得过氧化氢的水溶液,剩余溶液再循环使用。
①写出电解NH4HSO4溶液的化学方程式
②写出水解器中(NH4)2S2O8溶液的水解方程式 。
③铂价格昂贵,试分析电槽阳极用铂不用铅的原因 。
④试分析水解器中使用减压水解、蒸馏的原因 。
(2)在电解后的过硫酸铵溶液中加入硫酸氢钾,析出过硫酸钾固体,过硫酸钾具有强氧化性,常被还原为硫酸钾,80℃以上易发生分解。
①将0.40 mol过硫酸钾与0.20 mol硫酸配制成1 L溶液,在80 ℃条件下加热并在t时刻向溶液中滴加入少量FeCl3溶液,测定溶液中各成分的浓度如右图所示(H+浓度未画出)。图中物质X的化学式为 。
②已知硫酸锰(MnSO4)和过硫酸钾(K2S2O7)两种盐溶液在银离子催化下可发生反应,得到紫红色溶液。此反应的离子反应方程式 .
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省东阳市黎明补校高三12月月考化学试卷(解析版) 题型:填空题
(共12分)钛是21世纪金属。下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
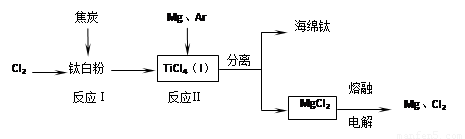
已知:① Mg(s)+Cl2 (g)=MgCl2 (s) △H=-641 kJ·mol-1
② Cl2(g)+1/2Ti (s)=1/2TiCl4 (l) △H=-385 kJ·mol-1
(1)钛白粉是利用TiO2+发生水解生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的。
TiO2+发生水解的离子方程式为 。
(2)反应I在800~900℃下进行,还生成一种可燃性无色气体,该反应的化学方程式为 ;
反应II的热化学方程式为 。
(3)该工艺流程中,可以循环使用的物质有 (填化学式)。
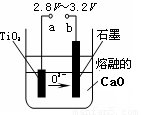
(4)在800℃~1000℃时电解TiO2也可制得海绵钛,装置如右图所示。图中b是电源的 极,阴极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2012届浙江省东阳市高三下学期期中考试化学试卷 题型:填空题
(12分)利用所学化学反应原理,解决以下问题:
(1)某溶液含两种相同物质的量的溶质,且其中只存在OH一、H+、NH4+、Cl一四种离子,
且c(NH4+)>c(Cl-)>c(OH-)>c(H+),则这两种溶质是 。
(2)0.1 mol·L-1的氨水与0.05 mol·L-1的稀硫酸等体积混合,用离子方程式表示混合后溶液的酸碱性: 。
(3)已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,则难溶盐RX、RY和R2Z的饱和溶液中,R+浓度由大到小的顺序是 。
(4)向20 mL硫酸和盐酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量
如右图所示,B点溶液的pH=7(假设体积
可以直接相加),则c(HCl)= mol·L-1.

(5)在温度、容积相同的3个密闭容器中,
按下表投入反应物,发生反应(H2(g)+
I2(g) 2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下, 测得反应达
2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下, 测得反应达
到平衡时的数据如下表:
下列说法正确的是 。
A. +
+ =1
B.2
=1
B.2 =
= C.a+b=14.9
D.c1=c2=c3
C.a+b=14.9
D.c1=c2=c3

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com