
分析 ①碳化硅是空间网状结构,为原子晶体,每个硅原子连接4个碳原子,形成正四面体结构;
②距离中心Si最近的第一层的4个C原子,每一个又连接着另外3个Si原子,这12个Si原子平均分布在一个球面上,根据直角三角形计算正四面体的边长.
解答 解:①碳化硅是空间网状结构,为原子晶体,每个硅原子连接4个碳原子,形成正四面体结构,其键角为109°28′,故答案为:原子;109°28′;
②距离中心Si最近的第一层的4个C原子,每一个又连接着另外3个Si原子,这12个Si原子平均分布在一个球面上,F是C原子,A、B、C、D分别代表一个Si原子,AB、AC、AD、BC、BD、CD的边长相等,AF、BF的长相等为d,F位于体心上,O位于正三角形BCD的重心上,在正三角形BCD中,BE为三角形BCD的高,则CE为BC的一半,如图 ,设正四面体的边长为x,CE的长为0.5x,BE=$\sqrt{{x}^{2}-(0.5x)^{2}}=\frac{\sqrt{3}}{2}x$,BO与OE的长之比为2:1,则BO的长为$\frac{\sqrt{3}}{2}x×\frac{2}{3}=\frac{\sqrt{3}}{3}x$,在三角形ABO中,AO的长=$\sqrt{{x}^{2}-(\frac{\sqrt{3}}{3}x)^{2}}=\frac{\sqrt{6}}{3}x$,在三角形BFO中,OF的长=$\frac{\sqrt{6}}{3}x-d$=$\sqrt{{d}^{2}-(\frac{\sqrt{3}}{3}x)^{2}}$,x=$\frac{2\sqrt{6}d}{3}$,
,设正四面体的边长为x,CE的长为0.5x,BE=$\sqrt{{x}^{2}-(0.5x)^{2}}=\frac{\sqrt{3}}{2}x$,BO与OE的长之比为2:1,则BO的长为$\frac{\sqrt{3}}{2}x×\frac{2}{3}=\frac{\sqrt{3}}{3}x$,在三角形ABO中,AO的长=$\sqrt{{x}^{2}-(\frac{\sqrt{3}}{3}x)^{2}}=\frac{\sqrt{6}}{3}x$,在三角形BFO中,OF的长=$\frac{\sqrt{6}}{3}x-d$=$\sqrt{{d}^{2}-(\frac{\sqrt{3}}{3}x)^{2}}$,x=$\frac{2\sqrt{6}d}{3}$,
故答案为:12;$\frac{2\sqrt{6}d}{3}$.
点评 本题考查了晶胞的计算、元素周期律、原子杂化等知识点,这些都是学习重点也是学习难点,同时考查学生的空间想象能力、分析问题能力、数学分析逻辑能力等,难度较大.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:解答题
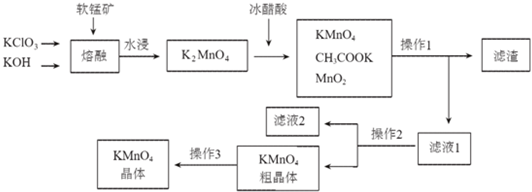
| 物质 温度 | KMnO4 | CH3COOK | K2SO4 | KCl |
| 20℃ | 6.34 | 217 | 11.1 | 34.2 |
| 90℃ | 45.2 | 398 | 22.9 | 53.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
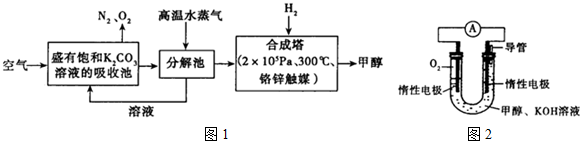
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数 | B. | 电子数 | C. | 中子数 | D. | 质量数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+的结构示意图: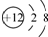 | |
| B. | 葡萄糖的结构简式:C6H12O6 | |
| C. | H2O2的电子式: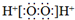 | |
| D. | 硫酸的电离方程式:H2SO4═H22++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
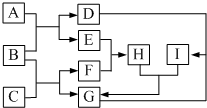 有关物质的转化关系如图所示(部分物质和条件已略去).F是最简单的烃,B是最常见的无色液体,A是一种淡黄色固体,G是一种既能溶于强酸又能溶于强碱的白色固体,C由两种短周期元素组成,其摩尔质量为144g•mol-1.
有关物质的转化关系如图所示(部分物质和条件已略去).F是最简单的烃,B是最常见的无色液体,A是一种淡黄色固体,G是一种既能溶于强酸又能溶于强碱的白色固体,C由两种短周期元素组成,其摩尔质量为144g•mol-1. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com