
【题目】(1)在一密闭容器中充入a mol NO和b mol O2,可发生如下反应:2NO+O2 = 2NO2,充分反应后容器中氮原子和氧原子的个数之比为________。
(2)某强氧化剂RO4- 能将Na2SO3氧化成Na2SO4,已知含2.0×103 mol RO4- 离子的溶液,恰好跟25.0 mL 0.2 mol/L 的Na2SO3溶液完全反应,则反应后R的化合价为_______价。
(3)按体积比为1∶2∶3所组成的N2、O2、CO2的混合气体100g,在标准状况下的体积为_____L。
【答案】a︰(a+2b) +2 60
【解析】
利用原子守恒即可求出氮原子和氧原子的个数比;利用氧化还原反应中氧化剂和还原剂得失电子数相同即可求出R的化合价;根据阿伏加德罗定律即在同温同压下,气体的体积之比等于其物质的量之比来求得混合气体的体积。
(1)根据原子守恒即化学反应前后各原子的数目不变,反应后容器中氮原子和氧原子的个数比等于反应前氮原子和氧原子的个数比= a︰(a+2b)。
(2)RO4- 中R的化合价为+7,设反应后R的化合价为x,25.0 mL 0.2 mol/L 的Na2SO3被氧化成Na2SO4,失去电子的物质的量n=0.025 L×0.2 mol/L×2=0.01 mol。在氧化还原反应中得失电子数相同即:2.0×103 mol×(7-x)=0.01 mol,解得x=+2,即反应后R的化合价为+2。
(3)在同温同压下,体积之比等于物质的量之比。设N2、O2、CO2的物质的量分别为x mol、2x mol、3x mol。可得;x mol×28 g/mol+2x mol×32 g/mol+3x mol×44 g/mol=100 g。
解得x=![]() 。所以标准状况下,混合气体的体积为(
。所以标准状况下,混合气体的体积为(![]() mol+2×
mol+2×![]() mol+3×
mol+3×![]() mol)×22.4 L/mol=60 L。
mol)×22.4 L/mol=60 L。


科目:高中化学 来源: 题型:
【题目】用硫及其化合物制硫酸有下列三种反应途径,某些反应条件和产物已省略。下列有关说法不正确的是( )
途径①:S![]() H2SO4
H2SO4
途径②:S![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
途径③:FeS2![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
A. 途径①的反应中体现了浓硝酸的强氧化性
B. 途径②、③的第二步反应在实际生产中可以通过增大氧气的浓度来降低成本
C. 由途径①、②、③分别制取1 mol 硫酸,理论上各消耗1 mol 硫,各转移6 mol 电子
D. 途径②、③比途径①污染相对小且原子利用率高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从海带中提取碘的操作过程中,仪器选用不正确的是 ( )
选项 | A | B | C | D |
操作 | 称取3g左右的剪碎了的干海带 | 灼烧干海带碎片至完全变成灰烬 | 过滤煮沸后的海带灰与水的混合液 | 用四氯化碳从氧化后的海带灰浸取液中提取碘 |
选用仪器 | 托盘天平 | 蒸发皿 | 普通漏斗 | 分液漏斗 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组采用刻蚀废液(主要含CuCl2、FeCl3、FeCl2、HCl)制取Cu和Cu2Cl2,实验流程如下:

已知:Cu2Cl2是白色固体,微溶于水,难溶于乙醇,受潮后在空气中易被迅速氧化。
(1)“预处理"时,需用Na2CO3调节溶被至微酸性而不是碱性,其原因是_____
(2)“还原Ⅰ”需在80℃条件下进行,适宜的加热方式为_______
(3)“还原Ⅱ”中,Cu2+参与反应的离子方程式为______
(4)“搅拌”时加入NaCl粉末的作用是________
(5)“过滤Ⅱ”得到的Cu2Cl2需用无水乙醇洗涤,并在真空干燥机内于70℃干燥2小时,冷却,密封包装。于70℃真空干燥的目的是_________
(6)①请设计从“过滤Ⅰ”所得滤渣中获取Cu的实验方案:_______(实验中可供选择的试剂:稀硫酸、稀硝酸、蒸馏水)。
②现欲测定途径a、b回收铜元素的回收率比,请补充实验方案:_______________,分别按途径a、b制取Cu和Cu2Cl2,测得Cu的质量为m1g,Cu2Cl2的质量为m2g,则途径a、b铜素的回收率比为________(铜元素回收率=产品中铜元素质量/废液中铜元素的质量×100%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,依次通过的洗气瓶中盛放的试剂最好为( )
A.澄清石灰水、浓硫酸B.KMnO4酸性溶液、浓硫酸
C.溴水、浓硫酸D.浓硫酸、KMnO4酸性溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过以下反应合成:Al2O3+N2+3C![]() 2AlN+3CO。有关该反应下列叙述正确的是
2AlN+3CO。有关该反应下列叙述正确的是
A. 上述反应中,N2是还原剂,Al2O3是氧化剂
B. AlN中氮的化合价为+3
C. 上述反应中,每生成1 molAlN需转移3 mol电子
D. AlN的摩尔质量为41 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。试运用所学知识,回答下列问题:
(1)已知在一定温度下,①C(s)+CO2(g) ![]() 2CO(g) △H1=a kJ/mol 平衡常数K1;
2CO(g) △H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g) ![]() H2(g)+CO2(g) △H2=b kJ/mol 平衡常数K2;
H2(g)+CO2(g) △H2=b kJ/mol 平衡常数K2;
某反应的平衡常数表达式K3=![]() ,请写出此反应的热化学方程式:__________,K1、K2、K3之间的关系是:_____________。
,请写出此反应的热化学方程式:__________,K1、K2、K3之间的关系是:_____________。
(2)将原料气按n(CO2):n(H2)=1:4置于密闭容器中发生CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)反应,测得H2O(g)的物质的量分数与温度的关系如图所示
CH4(g)+2H2O(g)反应,测得H2O(g)的物质的量分数与温度的关系如图所示
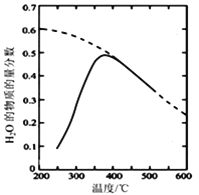 (虚线表示平衡曲线)。
(虚线表示平衡曲线)。
①该反应的平衡常数K随温度降低而________(填“增大”或“减小”)。
②在密闭恒温(高于100℃)恒容装置中进行该反应,下列能说明达到平衡状态的是_____。
A.混合气体密度不再改变
B.混合气体压强不再改变
C.混合气体平均摩尔质量不再改变
D. n(CO2):n(H2)=1:2
③200℃达到平衡时体系的总压强为p,该反应平衡常数Kp的计算表达式为______。(不必化简,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(3)500℃时,CO与水反应生成CO2和H2。将CO2和H2分离得到H2的过程示意图如下。
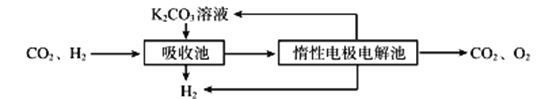
①吸收池中所有离子浓度的等式关系是____________________________。
②结合电极反应式,简述K2CO3溶液的再生原理:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】龙癸醛是一种珍贵香料,广泛应用于香料、医药、染料及农药等行业。其合成路线如图所示(部分反应产物和反应条件已略去)。

回答下列问题:
(1)下列有关R和烯烃C3H6的说法正确的是__________________。(填代号)
A.它们的实验式相同 B.它们都能使溴水褪色
C.它们都能发生加成反应 D.它们都含有碳碳双键
(2)反应⑤的试剂和条件是___________________________;反应③的类型是_____________________。
(3)T所含官能团的名称是________;反应④的化学方程式为__________________________________。
(4)X的名称是____________________。
(5)遇氯化铁溶液发生显色反应的T的同分异构体有________种,其中,在核磁共振氢谱上有4组峰且峰面积比为1∶2∶3∶6的结构简式为_______________________________________________。
(6)参照上述流程图,以2—甲基—1,3—丁二烯为原料,经三步制备2—甲基—1,4—丁二醛,设计合成路线:________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com