

| A�����ǻ�ѧ��ת��Ϊ���ܣ��ҡ����ǵ���ת��Ϊ��ѧ�� |
| B��C1��C2�ֱ���������������пƬ��C3�϶�����������Ӧ |
| C��C1��C3�ų���������ͬ��ͭƬ����Ƭ�ų�������Ҳ��ͬ |
| D��������Һ��pH�����ߣ��ҡ�������Һ��pH��С |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪ij���淴ӦmA��g��+n B��g��?pC��g������=Q���ܱ������н��У���ͼ�б�ʾ�ڲ�ͬ��Ӧʱ��tʱ���¶�T��ѹǿP�뷴Ӧ��B�ڻ�������еİٷֺ���B%�Ĺ�ϵ���ߣ������߷��������ж���ȷ�ģ�������
��֪ij���淴ӦmA��g��+n B��g��?pC��g������=Q���ܱ������н��У���ͼ�б�ʾ�ڲ�ͬ��Ӧʱ��tʱ���¶�T��ѹǿP�뷴Ӧ��B�ڻ�������еİٷֺ���B%�Ĺ�ϵ���ߣ������߷��������ж���ȷ�ģ�������| A��T1��T2 P1��P2 m+n��p Q��0 |
| B��T1��T2 P1��P2 m+n��p Q��0 |
| C��T1��T2 P1��P2 m+n��p Q��0 |
| D��T1��T2 P1��P2 m+n��p Q��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��OA�η�����Ӧ�����ӷ���ʽΪ��H++OH-�TH2O CO32-+H+�THCO3- |
| B��������35mL����ʱ������CO2�����Ϊ224mL |
| C��A����Һ�е�����ΪNaC1��NaHCO3 |
| D���������NaOH������0.60g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ | ����� | ����� | �ǵ���� | |
| A | ���� | ��ˮ����� | ���� | �ɱ� |
| B | ����ˮ | ������Һ | �Ȼ�ͭ | �������� |
| C | ���� | ���� | �� | ̼��� |
| D | ���� | ʳ��ˮ | ������ | ̼���� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1 mol?L-1NaOH��Һ��0.2 mol?L-1CH3COOH��Һ�������Ϻ�c��CH3COOH��+c��CH3COO-��=0.2 mol?L-1 |
| B�������£���CH3COONa��HCl����Һ��ϳ����Ե���Һ�У�c��Na+����c��Cl-��=c��CH3COOH�� |
| C��pH��ȵĢ�NH4Cl���ڣ�NH4��2SO4����NH4HSO4��Һ��c��NH4+����С˳��Ϊ��=�ڣ��� |
| D��25��ʱ��pH=a��������pH=b��Ba��OH��2��Һ�������Ϻ�ǡ����ȫ��Ӧ����a+b=14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������I��Ev�� | A | B | C | D | E | F |
| I1 | 11.3 | 14.5 | 13.6 | 5.2 | 7.6 | 6.0 |
| I2 | 24.4 | 29.6 | 35.1 | 49.3 | 15.0 | 18.8 |
| I3 | 47.9 | 47.4 | 54.9 | 71.6 | 80.1 | 28.4 |
| I4 | 64.5 | 77.5 | 77.4 | 98.9 | 109.2 | 112.0 |
| I5 | 392.1 | 97.9 | 113.9 | 138.3 | 141.3 | 153.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ʳƷ���Ӽ���ʳ������彡�����к� |
| B����ͨ�����͵������մɶ������������ǽ������� |
| C�������ƹ�Ӧ��ȼ�ϡ������������������ɼ�����������͵�������Կ�������Ⱦ |
| D��Ϊ������ȱ�����������涨��ʳ���б�������һ������KI |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������CO2Ũ�ȵij����߸��Ѿ��������ǵĸ߶����ӣ���ѧ����ָ�������ж�����̼�ij�������������ʹȫ���ů�������ȫ�ı��ź�ˮ���ܽ����̼��CO2��HCO3-��CO32-����Ũ����������й�������ŵ����2020�꣬��λGDP������̼�ŷű�2005���½�40%��50%��
������CO2Ũ�ȵij����߸��Ѿ��������ǵĸ߶����ӣ���ѧ����ָ�������ж�����̼�ij�������������ʹȫ���ů�������ȫ�ı��ź�ˮ���ܽ����̼��CO2��HCO3-��CO32-����Ũ����������й�������ŵ����2020�꣬��λGDP������̼�ŷű�2005���½�40%��50%��| 1 |
| 2 |
| 3 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� ���װ�������� |
B��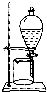 �ӵ��CCl4��Һ�з������ |
C�� ��ȥ�����е���ϩ |
D�� ����ױ����Ҵ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com