
| A、①>② | B、①<② |
| C、①=② | D、不能确定 |


科目:高中化学 来源: 题型:
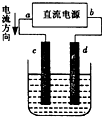
| A、电解过程中,d电极质量增加 |
| B、a为阳极、b为阴极 |
| C、a为负极、b为正极 |
| D、电解过程中,氯离子浓度基本不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
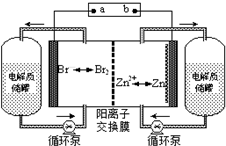
| A、充电时电极b连接电源的正极 |
| B、阳离子交换膜可阻止Br2与Zn直接发生反应 |
| C、放电时正极的电极反应式为Zn-2e-═Zn2+ |
| D、充电时左侧电解质储罐中的离子总浓度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生成40.0 L N2(标准状况) |
| B、有0.250 mol KNO3被氧化 |
| C、转移电子的物质的量为1.75mol |
| D、被氧化的N原子的物质的量为3.75mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、431 kJ/mol |
| B、945.6 kJ/mol |
| C、649 kJ/mol |
| D、869 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解精炼铜时,当阳极上质量减少6.4g时,电路上转移的电子数目为0.2 NA |
| B、1L 1.0mol?L-1NH4Cl与2L 0.5mol?L-1NH4HSO4溶液含NH4+数目相同 |
| C、0.2mol Zn与一定量浓H2SO4恰好完全反应,生成的气体分子数必为0.2NA |
| D、将2mL0.5 mol?Lˉ1Na2SiO3溶液滴入稀盐酸中制得H4 SiO4胶体,所含胶粒数为0.001NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、P(HCl)>P(H2S)>P(O2) |
| B、P(O2)>P(H2S)>P(HCl) |
| C、P(H2S)>P(HCl)>P(O2) |
| D、P(H2S)>P(O2)>P(HCl) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com