
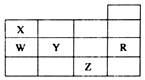
 五种前四周期元素X、Y、Z、W、R在元素周期表中的位置如图所示.下列有关元素的叙述中,正确的是( )
五种前四周期元素X、Y、Z、W、R在元素周期表中的位置如图所示.下列有关元素的叙述中,正确的是( )| A. | W的简单氢化物的沸点比X的简单氢化物的沸点低 | |
| B. | 五种元素均在元素周期表的s区 | |
| C. | 电负性和第一电离能均为:Y>X>W | |
| D. | 五种元素的单质中Z的单质的沸点最高 |
分析 由前四周期元素X、Y、Z、W、R在元素周期表中的位置可知,R为Ar,X为N,W为P,Y为S,Z为Br,
A.氨气分子间含氢键;
B.最后填充的均为p电子;
C.非金属性越强,电负性越大,第一电离能越大,但p电子半满为稳定结构;
D.常温下Z的单质为液体,而W、Y的单质为固体.
解答 解:由前四周期元素X、Y、Z、W、R在元素周期表中的位置可知,R为Ar,X为N,W为P,Y为S,Z为Br,
A.氨气分子间含氢键,则W的简单氢化物的沸点比X的简单氢化物的沸点低,故A正确;
B.原子的电子排布中最后填充的均为p电子,则均为p区元素,故B错误;
C.非金属性越强,电负性越大,第一电离能越大,但p电子半满为稳定结构,则电负性为X>Y>W,第一电离能为X>W>Y,故C错误;
D.常温下Z的单质为液体,而W、Y的单质为固体,则元素的单质中沸点最高的不是Z的单质,故D错误;
故选A.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、电子排布为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:选择题

| A. | 反应在2~4min内平均反应速率最大 | |
| B. | 一段时间后,反应速率减小的原因是c(H+)减小 | |
| C. | 反应开始4min内温度对反应速率的影响比浓度大 | |
| D. | 反应在2~4min内生成CO2的平均反应速率为v(CO2)=0.06mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝制容器可用于盛放稀硫酸 | |
| B. | 氯化铁溶液可用于制作印刷电路铜板 | |
| C. | 碳酸钡可用作医疗上的“钡餐” | |
| D. | 氢氧化钠可用作治疗胃酸过多的药物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去油脂中的少量水分,旣可以用无水硫酸钠也可以用碱石灰 | |
| B. | 葡萄糖、蔗糖、淀粉、纤维素的形态不同,在水中的溶解性相似 | |
| C. | 一定条件下,氨基酸之间能发生反应合成更复杂的化合物(多肽),构成蛋白质 | |
| D. | 向鸡蛋清的溶液中加入饱和(NH4)2SO4溶液,鸡蛋清因发生变性而析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钡和硫酸铜溶液的反应:Ba+CuSO4═BaSO4↓+Cu | |
| B. | 过氧化钡的化学式为Ba2O2 | |
| C. | 反应Na2O2+2HCl═2NaCl+H2O2为氧化还原反应 | |
| D. | 过氧化钡和过氧化钠都具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是
如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是 | A. | 铜屑和稀硝酸 | B. | 碳酸钙和稀盐酸 | ||
| C. | 二氧化锰和浓盐酸 | D. | 氧化钙和浓氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | l8gNH4+中所含的电子数为11NA | |
| B. | 常温下,1L PH=1的H2SO4溶液中含有的H+的数目为0.2NA | |
| C. | 标准状况下,22.4LCl2完全溶于水时形成氯水时,转移电子数为NA | |
| D. | 常温常压下,3.4gH2O2含有极性键的数目为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com