
| A£® | [H+]=[OH-]µÄČÜŅŗ | B£® | pH£¼7µÄČÜŅŗ | ||
| C£® | [H+]=1.0”Į10-7mol•L-1 µÄČÜŅŗ | D£® | [H+]£¾[OH-]µÄČÜŅŗ |
·ÖĪö ČÜŅŗÖŠc£ØH+£©=c£ØOH-£©£¬ŌņČÜŅŗ³ŹÖŠŠŌ£¬Čē¹ūc£ØH+£©£¾c£ØOH-£©£¬ČÜŅŗ³ŹĖįŠŌ£¬Čē¹ūc£ØH+£©£¼c£ØOH-£©£¬ČÜŅŗ³Ź¼īŠŌ£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗA£®c£ØH+£©=c£ØOH-£©µÄČÜŅŗ³ŹÖŠŠŌ£¬¹ŹA“ķĪó£»
B£®Čē100”ꏱ“æĖ®pH=6£¬ŌņpH£¼7µÄČÜŅŗ²»Ņ»¶Ø³ŹĖįŠŌ£¬æÉÄܳŹÖŠŠŌ»ņ¼īŠŌ£¬¹ŹB“ķĪó£»
C£®c£ØH+£©=1”Į10-7 mol•L-1æÉÄܳŹÖŠŠŌ”¢æÉÄܳŹĖįŠŌ»ņ¼īŠŌ£¬¹ŹC“ķĪó£»
D£®c£ØH+£©£¾c£ØOH-£©µÄČÜŅŗ³ŹĖįŠŌ£¬c£ØH+£©=c£ØOH-£©µÄČÜŅŗ³ŹÖŠŠŌ£¬c£ØH+£©£¼c£ØOH-£©µÄČÜŅŗ³Ź¼īŠŌ£¬¹ŹDÕżČ·£¬
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĢ½¾æČÜŅŗĖį¼īŠŌ£¬ĪŖøßæ¼øßʵµć£¬øł¾ŻČÜŅŗÖŠc£ØH+£©”¢c£ØOH-£©µÄĻą¶Ō“óŠ”ÅŠ¶ĻČÜŅŗĖį¼īŠŌ£¬²»ÄÜøł¾ŻČÜŅŗpH¶ØŠŌÅŠ¶ĻĖį¼īŠŌ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 Óū²ā¶ØijNaOHČÜŅŗµÄĪļÖŹµÄĮæÅØ¶Č£¬æÉÓĆ0.1000mol•L-1HCl±ź×¼ČÜŅŗ½ųŠŠÖŠŗĶµĪ¶Ø£ØÓĆ·ÓĢŖ×÷ÖøŹ¾¼Į£©£®
Óū²ā¶ØijNaOHČÜŅŗµÄĪļÖŹµÄĮæÅØ¶Č£¬æÉÓĆ0.1000mol•L-1HCl±ź×¼ČÜŅŗ½ųŠŠÖŠŗĶµĪ¶Ø£ØÓĆ·ÓĢŖ×÷ÖøŹ¾¼Į£©£®| ŹµŃéŠņŗÅ | “ż²āNaOHČÜŅŗµÄĢå»ż/mL | 0.1000mol•L-1HClČÜŅŗµÄĢå»ż/mL | |
| µĪ¶ØĒ°æĢ¶Č | µĪ¶ØŗóæĢ¶Č | ||
| 1 | 25.00 | 0.00 | 26.11 |
| 2 | 25.00 | 1.56 | 31.30 |
| 3 | 25.00 | 0.22 | 26.31 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŅŃÖŖ£¬AŹĒ³£¼ūµÄ½šŹōµ„ÖŹ£¬ÓėBµÄĖ®ČÜŅŗ·“Ӧɜ³ÉCŗĶD£®D”¢FŹĒĘųĢåµ„ÖŹ£¬DŌŚFÖŠČ¼ÉÕŹ±²śÉś²Ō°×É«»šŃę£®A”¢B”¢C”¢D”¢E”¢FĮłÖÖĪļÖŹµÄĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø·“Ó¦Ģõ¼ž¼°²æ·Ö²śĪļĪ“ĮŠ³ö£©
ŅŃÖŖ£¬AŹĒ³£¼ūµÄ½šŹōµ„ÖŹ£¬ÓėBµÄĖ®ČÜŅŗ·“Ӧɜ³ÉCŗĶD£®D”¢FŹĒĘųĢåµ„ÖŹ£¬DŌŚFÖŠČ¼ÉÕŹ±²śÉś²Ō°×É«»šŃę£®A”¢B”¢C”¢D”¢E”¢FĮłÖÖĪļÖŹµÄĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø·“Ó¦Ģõ¼ž¼°²æ·Ö²śĪļĪ“ĮŠ³ö£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś | B£® | ¢Ł¢Ü | C£® | ¢Ś¢Ū | D£® | ¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
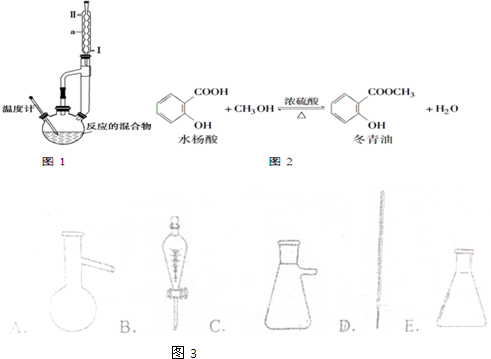
| Ļą¶Ō·Ö ×ÓÖŹĮæ | ĆܶČ/g•cm-3 | ·Šµć/”ę | ČܽāŠŌ | |
| ¶¬ĒąÓĶ | 152 | 1.180 | 222.2 | Ī¢ČÜÓŚĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4 L HClČÜÓŚĖ®ŗóČÜŅŗÖŠŗ¬ÓŠnAøöHCl·Ö×Ó | |
| B£® | 1L 0.1 mol•L-1µÄNa2SO4ČÜŅŗÖŠŗ¬ÓŠ0.2 nAøöNa+ | |
| C£® | 1 mol ĮņĖį¼ŲÖŠŅõĄė×ÓĖł“ųµēŗÉŹżĪŖnA | |
| D£® | ½«0.1molĀČ»ÆĢśČÜÓŚ1LĖ®ÖŠ£¬ĖłµĆČÜŅŗŗ¬ÓŠ0.1nAFe3+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3£ŗ1 | B£® | 3£ŗ2 | C£® | 2£ŗ1 | D£® | 1£ŗ2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ōö¼ÓSO2µÄÅØ¶Č | B£® | ³äČėŅ»¶ØĮæ¶čŠŌĘųĢå | ||
| C£® | ÉżøßĪĀ¶Č | D£® | Ź¹ÓĆ“ß»Æ¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
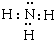 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com