
【题目】若aAm+与bBn-的核外电子排布相同,则下列关系不正确的是( )
A.离子半径aAm+<bBn-
B.原子半径A<B
C.A的原子序数比B的原子序数大(m+n)
D.b=a-n-m
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】硝酸铵简称硝铵,可用作化肥,含氮量高。它在发生某些反应时既放出大量热又生成大量气体而爆炸,也可作炸药使用。
(1)硝铵受热:NH4NO3→N2O↑+2H2O,该反应中因为有____而属于氧化还原反应,其中发生还原过程元素的变化为___。
(2)硝铵受撞击:2NH4NO3→O2+2N2+4H2O,请在该反应方程式上补齐电子转移的方向和数目___。若反应中转移电子数为3.01×1024,则反应产生的气体在标准状况下的体积为____。
(3)一定温度下,硝铵分解:___NH4NO3→___HNO3+___N2↑+___H2O,配平该反应方程式,把系数填入对应的位置上。反应中被氧化与被还原的原子的物质的量之差为5mol时,参加反应的硝铵的质量为___。
(4)硝铵易溶于水,溶解时溶液的温度降低。硝铵溶于水时,温度降低的原因是_____,该水溶液呈(填“酸”“碱”或“中”)____性,用离子方程式表示原因为_____。
(5)为使该水溶液在常温下的pH为7,并不引入杂质,可以_____,试证明所得的溶液中c(NH4+)=c(NO3-):_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于元素周期表中下列位置的①~⑩十种元素,请回答有关问题(用元素符号或化学式回答)。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | ⑥ | ||||
3 | ⑦ | ⑧ | ⑨ | ⑩ |
(1)在上述元素中,金属性最强的是___,原子半径最大的是___(0族除外)。
(2)用电子式表示⑦和⑩形成的化合物的过程___。
(3)表中元素构成10电子微粒的分子有:___(任写2种)。
(4)⑤和⑨分别与氢原子构成的简单氢化物中沸点最高的是___。
(5)表中元素⑤和⑦可以形成一种淡黄色物质X,写出X的电子式:___,该物质所含化学键类型___,0.1molX与水反应转移电子数为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下列8组物质或粒子:
①14N和14C
②16O和18O
③氰酸铵(NH4CNO)与尿素[CO(NH2)2]
④足球烯(C60)和金刚石
⑤CH3CH2CH2CH3和CH(CH3)3
⑥CH3CH2CH3和CH3(CH2)2CH3
⑦![]() 和
和![]()
⑧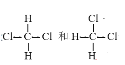
(1)互为同素异形体的是____________(填编号,下同),
(2)互为同位素的是____________,
(3)互为同系物的是____________,
(4)互为同分异构体的是____________。
Ⅱ.回答下列有关有机化学的问题:
(5)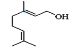 的分子式为____________,该物质所含官能团名称是____________。
的分子式为____________,该物质所含官能团名称是____________。
(6)苯与浓硫酸和浓硝酸混合加热产生硝基苯的反应方程式为____________,反应类型是____________。
(7)下列能使酸性高锰酸钾溶液褪色的是____________。
A.乙醇 B.聚乙烯 C.苯 D.甲苯 E.戊烷 F.苯乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 第三电子层(最外层 )上有6个电子 |
X | 核内质子数为6 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
W | 其单质既能跟酸反应,又能跟碱反应,都产生H2 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是_______。
(2)元素Y与氢元素形成一种离子![]() ,写出该微粒的化学式:____(用元素符号表示)。
,写出该微粒的化学式:____(用元素符号表示)。
(3)元素Z与元素T相比,非金属性较强的是____(用元素符号表示 ),下列表述中能证明这一事实的是____(填序号 )。
①常温下Z的单质和T的单质状态不同
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4 )探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是____(填化学式 ),理由是____________。Z的最高价氧化物对应的水化物与W的最高价氧化物对应的水化物反应的离子方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究Na、Mg、Al活动性顺序,某课外小组同学进行了如下实验:
实验步骤 | 1.将一小块金属钠放入滴有酚酞溶液的冷水中。 2.将一小段用砂纸打磨后的镁带放入试管中,加入少量水,加热至水沸腾,冷却后,向试管中滴加酚酞溶液。 3.将一小段镁带投入稀盐酸中。 4.将一小片铝投入稀盐酸中。 |
他们记录的实验现象有:
实验现象 | ①剧烈反应,迅速生成大量的气体。 ②浮在水面上,熔成小球,不断游动,小球渐小最终消失,溶液变红。 ③反应不剧烈,产生无色气体。 ④有气体产生,溶液变成红色。 |
请帮助该小组同学补充下列实验报告中的内容。
(1)在下表中填写与实验步骤相对应的实验现象序号。
实验步骤 | 1 | 2 | 3 | 4 |
实验现象 | _____ | _____ | _____ | _____ |
(2)写出镁与水反应的化学方程式: _____。
(3)实验结论是: Na、Mg、Al金属性逐渐_____。
(4)用原子结构理论对上述实验结论进行解释:同周期元素从左至右,原子的电子层数相同,核电荷数逐渐增多,原子半径逐渐_____,原子核对电子的引力逐渐增强,失电子能力逐渐减弱,因此_____逐渐减弱。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得浓度均为0.5 molL-1的Pb(CH3COO)2溶液的导电性明显弱于Pb(NO3)2溶液,又知PbS是不溶于水及稀酸的黑色沉淀,下列离子方程式书写错误的是
A.Pb(NO3)2溶液与 CH3COONa 溶液混合:Pb2++2CH3COO-= Pb(CH3COO)2
B.Pb(NO3)2 溶液与K2S溶液混合:Pb2++S2-=PbS↓
C.Pb(CH3COO)2 溶液与K2S溶液混合:Pb2++S2- =PbS↓
D.Pb(CH3COO)2 在水中电离: Pb(CH3COO)2![]() Pb2+ +2CH3COO-
Pb2+ +2CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】少量铁粉与![]() 的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变
的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变![]() 的产量,可以使用如下方法中的( )
的产量,可以使用如下方法中的( )
①加水②加![]() 固体③滴入几滴浓盐酸④加
固体③滴入几滴浓盐酸④加![]() 固体⑤加
固体⑤加![]() 溶液⑥滴入几滴硫酸铜溶液⑦适当升高温度(不考虑盐酸挥发)
溶液⑥滴入几滴硫酸铜溶液⑦适当升高温度(不考虑盐酸挥发)
A.①⑥⑦B.③⑦C.③⑤D.⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】装置Ⅰ是实验室常见的装置,用途广泛(用序号或字母填空)。
(1)用它作为气体收集装置:若从a端进气可收集的有___,若从b端进气可收集的气体有___。
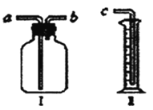
①O2 ②CH4 ③CO2 ④CO ⑤H2 ⑥N2 ⑦NH3
(2)用它作为洗气装置。若要除去CO2气体中混有的少量水蒸气,则广口瓶中盛放___,气体应从____端通入。
(3)将它与装置Ⅱ连接作为量气装置。将广口瓶中装满水,用乳胶管连接好装置,从___端通入气体。
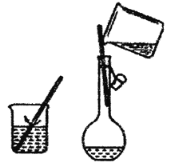
(4)某实验需要用1.0molL-1NaOH溶液500mL。配制实验操作步骤有:
a.在天平上称量NaOH固体,加水溶解,冷却至室温。
b.把制得的溶液小心地注入一定容积容量瓶中。
c.继续向容量瓶中加水至距刻度线1cm~2cm处,改用胶头滴管加水至刻度线。
d.用少量水洗涤烧杯和玻璃棒2~3次,每次将洗涤液转入容量瓶,并摇匀。
e.将容量瓶塞塞紧,充分摇匀。
填写下列空白:
①配制该溶液应当称取___克NaOH固体。
②操作步骤和正确顺序为____。
③如图该配制过程中两次用到玻璃棒,其作用分别是____、___。
④定容时,若俯视刻度线,会使结果____(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com