
【题目】下列关于浓硫酸的叙述,正确的是( )
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g) 达到平衡。下列说法正确的是( )
CH3OH(g) 达到平衡。下列说法正确的是( )
容器 | 温度/K | 物质的起始浓度/mol·L-1 | 物质的平衡浓度/mol·L-1 | ||
c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
Ⅱ | 400 | 0.40 | 0.20 | 0 | |
Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
A. 该反应的正反应吸热
B. 达到平衡时,容器Ⅱ中c(CH3OH)小于容器Ⅰ中c(CH3OH) 的两倍
C. 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分子中既有σ键,又有π键的是( ) ①HCl②H2O③N2④H2O2⑤C2H4⑥C2H2 .
A.①②③
B.③④⑤⑥
C.①③⑥
D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】强酸溶液A与强碱溶液B,在常温下其pH之和为15,当它们按一定体积比混合时,溶液的pH恰好为7,则A与B的体积比为
A. 1 : 1 B. 2 : 1 C. 1 : 10 D. 10 : 1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1 mol/L的H2C2O4溶液中H2C2O4、HC2O4-、C2O42-三者中所占物质的量分数(分布系数)随pH变化的关系如图所示。下列表述不正确的是
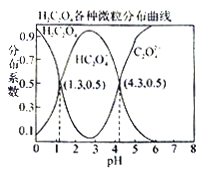
A. HC2O4-![]() H++C2O42-,K=1×10-4.3
H++C2O42-,K=1×10-4.3
B. 将等物质的量的NaHC2O4、Na2C2O4溶于水中,所得溶液pH恰好为4.3
C. 常温下HF的K=1×10-3.45,将少量H2C2O4溶液加入到足量NaF溶液中,发生的反应为:H2C2O4+F-=HF+HC2O4-
D. 在0.1 mol/LNaHC2O4溶液中,各离子浓度大小关系为:c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
A. 2.8g![]() 中含有的碳原子数为0.2NA
中含有的碳原子数为0.2NA
B. 标准状况下,5.6L四氯化碳含有的分子数为0.25NA
C. 乙烷和丙烯的物质的量共1mol,完全燃烧生成水分子数为3NA
D. 1mol苯分子中含有![]() 双键数为3NA
双键数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组设计如图装置制备干燥纯净的氯气,并验证氯气的性质。
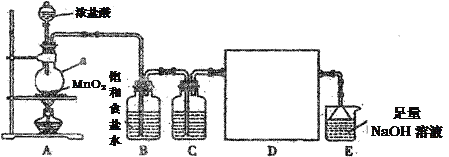
(1)仪器a的名称是____________________。
(2)B装置中试剂的作用是________________,C装置中的试剂为________________。
(3)D处方框内氯气的收集装置可选用____________(填写序号)。
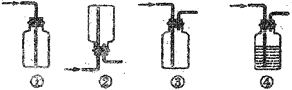
(4)将氯气通入如图装置中,充分反应后,静置,观察到的现象为________________;分离反应产物的实验操作名称为____________,需要的玻璃仪器有____________________。
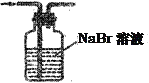
(5)实验结束后,E装置中氯元素的存在形式除了ClO-外,还有________(填写离子符号),请设计实验证明该离子的存在:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定条件下,体积为2L的密闭容器中,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0 mol和6.0 mol,3min后达到平衡,生成NH3的物质的量是2.4 mol。试求:
2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0 mol和6.0 mol,3min后达到平衡,生成NH3的物质的量是2.4 mol。试求:
① 3min内用N2表示的化学反应速率为____________。②H2的转化率是____________。
(2)某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。

a.实验室用装置E制备Cl2,其反应的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O。若有6 mol 的HCl参加反应,则转移的电子物质的量为____________;
MnCl2+Cl2+2H2O。若有6 mol 的HCl参加反应,则转移的电子物质的量为____________;
b.①反应开始一段时间后,观察到D试管中的品红溶液出现的现象是:
D:_____________________________________________________________。
②停止通气后,再给B、D两个试管分别加热;两个试管中的现象分别为:
B:____________________________________,D:________________________________。
c.另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com