

| A. | ②③ | B. | ③④ | C. | ①③ | D. | ②④ |
 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:实验题
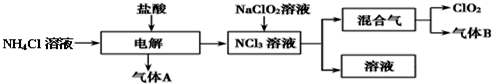
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种 | B. | 五种 | C. | 六种 | D. | 七种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
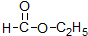 酯; ②
酯; ②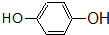 酚;
酚;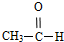 醛;④
醛;④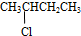 卤代烃;⑤
卤代烃;⑤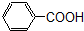 羧酸;
羧酸;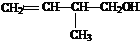
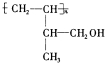 .
. +Cl2→CH2ClCHClCH(CH3)CH2OH.
+Cl2→CH2ClCHClCH(CH3)CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PbO2是电池的负极 | |
| B. | PbO2得电子,被氧化 | |
| C. | 电池放电时,溶液酸性增强 | |
| D. | 负极的电极反应式为:Pb+SO42--2e -═PbSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某同学用铁、铜作为电极,稀硫酸作为电解液组成原电池,如图所示,完成下列空格.(涉及到电极填写具体物质的元素符号)
某同学用铁、铜作为电极,稀硫酸作为电解液组成原电池,如图所示,完成下列空格.(涉及到电极填写具体物质的元素符号)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 | |
| B. | 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 | |
| C. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| D. | 向某溶液中加入硝酸酸化的氯化钡溶液,若生成白色沉淀,溶液中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
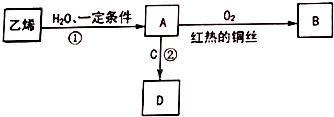 乙烯是一种重要的化工原料,可进行如图转化,其中C是食醋的主要成分.(部分反应物、生成物和反应条件已略去)
乙烯是一种重要的化工原料,可进行如图转化,其中C是食醋的主要成分.(部分反应物、生成物和反应条件已略去) CH3COOCH2CH3+H2O,反应类型是酯化反应,反应后可用饱和碳酸钠溶液除去D中混有的C.
CH3COOCH2CH3+H2O,反应类型是酯化反应,反应后可用饱和碳酸钠溶液除去D中混有的C.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com