
| A. | 等于20% | B. | 大于20% | C. | 小于20% | D. | 无法计算 |
分析 氨水浓度越大密度越小.等体积相混合时,浓度较稀的氨水质量较大,而较浓的氨水的质量较小,根据公式溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%计算.
解答 解:设:设35%的氨水和5%的氨水各取VL,密度分别是ρ1、ρ2,氨水浓度越大密度越小,所以ρ1<ρ2,则混合后的氨水的质量分数:
设这两种溶液的体积是V.则$\frac{35%ρ{\;}_{1}+5%ρ{\;}_{2}}{ρ{\;}_{1}V+ρ{\;}_{2}V}$×100%,根据ρ1<ρ2,所以混合所得氨水溶液的质量分数小于20%,
故选C.
点评 本题考查了有关溶质质量分数的简单计算,难度中等,①密度比水大的两种不同浓度溶液混合,等体积混合后所得溶液中溶质的质量分数大于等质量混合后所得溶液中溶质的质量分数(即两种溶液中溶质的质量分数之和的一半).如氢氧化钠、氯化钠溶液等.同理有:②密度比水小的两种不同浓度溶液混合,等体积混合后所得溶液中溶质的质量分数小于等质量混合后所得溶液中溶质的质量分数(即两种溶液中溶质的质量分数之和的一半).如氨水、酒精溶液等.


科目:高中化学 来源: 题型:选择题
| A.制取氨气 | B.制取NaHCO3 | C.分离NaHCO3 | D.干燥NaHCO3 |
 |  | 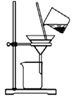 | 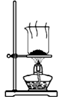 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
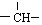 和一个-Cl,它的可能结构有四种,请写出它们的结构简式:CH3CH2CH2CHClCH3、CH3CH2CHClCH2CH3、CH3CH(CH3)CH2CH2Cl、CH2ClCH(CH3)CH2CH3.
和一个-Cl,它的可能结构有四种,请写出它们的结构简式:CH3CH2CH2CHClCH3、CH3CH2CHClCH2CH3、CH3CH(CH3)CH2CH2Cl、CH2ClCH(CH3)CH2CH3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Ⅰ红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题:
Ⅰ红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
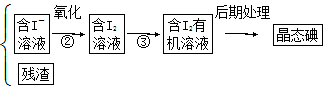
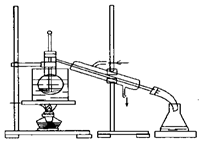
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 1 mol阿司匹林最多可消耗2 mol NaOH | |
| B. | 阿司匹林的分子式为C9H10O4 | |
| C. | 水杨酸可以发生取代、加成、氧化、加聚反应 | |
| D. | 服用阿司匹林,身体出现水杨酸不良反应时,可静脉注射NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
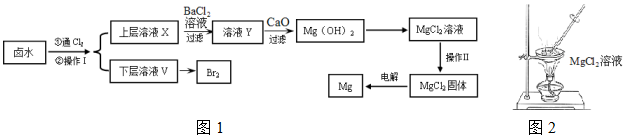
| 开始沉淀时 | 沉淀完全时 | |
| Mg2+ | pH=9.6 | pH=11.0 |
| Ca2+ | pH=12.2 | c(OH-)=1.8mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com