
 在下面的装置中,A是Cl2发生装置,C、D为气体净化装置,C中装有饱和NaCl溶液,D中装有浓H2SO4;E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶;烧杯G为尾气吸收装置.
在下面的装置中,A是Cl2发生装置,C、D为气体净化装置,C中装有饱和NaCl溶液,D中装有浓H2SO4;E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶;烧杯G为尾气吸收装置.
| ||
| ||
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
| A、滤出的不溶物一定是铜 |
| B、滤出的不溶物一定含铜,但不一定含铁 |
| C、滤出的不溶物一定是铁 |
| D、滤液中一定含有Fe2+和Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

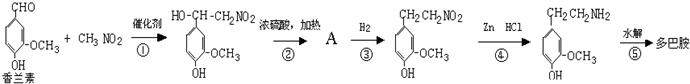 (3)多巴胺可由香兰素与硝基甲烷缩合,再经锌-盐酸还原水解而得.合成过程表示如下:
(3)多巴胺可由香兰素与硝基甲烷缩合,再经锌-盐酸还原水解而得.合成过程表示如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、属于非极性分子 |
| B、沸点低于CO2 |
C、电子式为 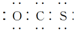 |
| D、三个原子位于同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温 |
| Al2O3 | Fe2O3 | Na2O | |
| 质量分数 | 0.065 | 0.850 | 0.029 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com