
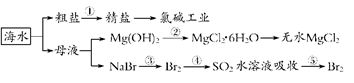
| A.工段③④⑤是溴元素的富集过程,③④⑤中均发生了氧化还原反应 |
| B.工段②中结晶出的MgCl2·6H2O可在空气中受热分解制无水MgCl2 |
| C.氯碱工业通过电解NaCl溶液,主要生产Cl2、H2和纯碱 |
| D.工段①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,操作顺序为:加入足量BaCl2溶液→加入足量NaOH溶液→加入足量Na2CO3溶液→加入足量盐酸→过滤 |
科目:高中化学 来源:不详 题型:单选题
| A.加入稀盐酸产生无色无味气体,将气体通入石灰水中,变浑浊,一定有CO32- |
| B.加入BaCl2溶液产生白色沉淀,再加上稀盐酸沉淀不消失,一定有SO42- |
| C.加入足量稀盐酸无沉淀,再加BaCl2溶液有白色沉淀,一定有SO42- |
| D.加入Na2CO3溶液产生白色沉淀,再加稀盐酸白色沉淀消失,一定有Ba2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
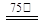 ZnFe2(C2O4)3·6H2O↓……………(a)
ZnFe2(C2O4)3·6H2O↓……………(a) ZnFe2O4 + 2CO2↑+4CO↑+6H2O ……………(b)
ZnFe2O4 + 2CO2↑+4CO↑+6H2O ……………(b)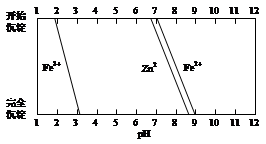
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验步骤 | 实验操作 | 现象与结论 | 离子方程式 |
| 第1步 | 取2~3mL溶液装于试管,向试管中滴加几滴KSCN溶液 | | |
| 第2步 | | 若溶液紫色褪去,则溶液 含有Fe2+;若无明显变化, 则不含Fe2+ | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
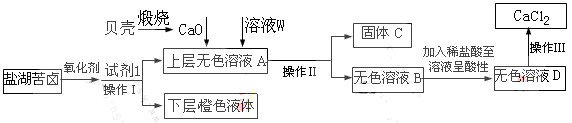
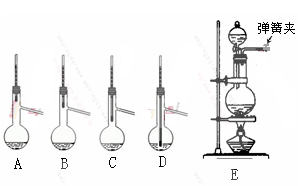
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
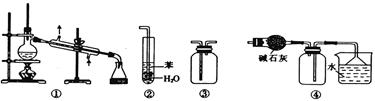
| A.装置③可用于收集H2、CO2、Cl2、NH3等气体 |
| B.装置②可用于吸收NH3或HCl气体,并防止倒吸 |
| C.装置①常用于分离互不相溶的液体混合物 |
| D.装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
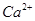 、
、 、
、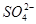 ,可先将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液。下列操作顺序正确的是
,可先将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液。下列操作顺序正确的是| A.②⑤④①③ | B.⑤②①④③ |
| C.①④②⑤③ | D.④①②⑤③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com