
A��B��C�����ֳ���������Ԫ�صĵ��ʡ�������DΪ��ɫҺ�壬E��һ�ֳ������������塣��ת����ϵ��ͼ(��Ӧ�����Ͳ��ֲ�����ȥ)���Իش�
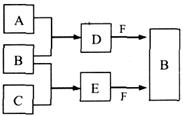
��1��E�ĵ���ʽ�� ��
��2������X��B��D���ܷ�Ӧ���ɺ�ɫ����Y��Y�Ļ�ѧʽ�� ��
��3������Z�����ڶԿ�������ɱ����������ˮ�����ʵȡ�Z��B�����Ԫ����ͬ��Z�����и�ԭ������������֮��Ϊ18��Z�����Ե⻯����Һ��Ӧ����B�͵ⵥ�ʣ���Ӧ�����ӷ���ʽ�� ��
��4��ȡ0.3 mol F������D��ֻ�Ϻ�������Һ����ͨ��0.2 mol E��ַ�Ӧ�����õ���ˮ��Һ�и������ӵ�Ũ���ɴ�С��˳����(������H+) ��
��5��E�Ĵ����ŷŻ������ܶ�����⡣�п�ѧ���������E��H2�ϳ�CH3OH��H2O����E�����ۺ����á�25�棬101 kPaʱ���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
(��֪�״���ȼ����![]() ��������ȼ����
��������ȼ����![]() )
)
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
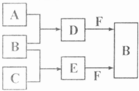 A��B��C�����ֳ���������Ԫ�صĵ��ʣ�������DΪ��ɫҺ�壬E��һ�ֳ������������壮��ת����ϵ��ͼ����Ӧ�����Ͳ��ֲ�����ȥ�����Իش�
A��B��C�����ֳ���������Ԫ�صĵ��ʣ�������DΪ��ɫҺ�壬E��һ�ֳ������������壮��ת����ϵ��ͼ����Ӧ�����Ͳ��ֲ�����ȥ�����Իش�



�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
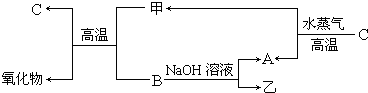
 �ס��ҡ������ֳ������ʣ�A��B��C�����ֳ����Ļ����AΪ����ɫ���壻����֮���ת����ϵ��ͼ��ʾ������д���пհף�
�ס��ҡ������ֳ������ʣ�A��B��C�����ֳ����Ļ����AΪ����ɫ���壻����֮���ת����ϵ��ͼ��ʾ������д���пհף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
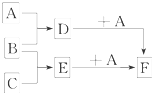 ��֪A��B��C�����ֳ����ĵ��ʣ�����AΪ���壬B��CΪ���壻D�ı�����Һ�����ˮ�м�����У���Һ�ʺ��ɫ��B��C��Ӧʱ�ɹ۲쵽��ɫ���棬����K������ˮ����ɫ��ҺE������֮��ת����ϵ��ͼ��ʾ��
��֪A��B��C�����ֳ����ĵ��ʣ�����AΪ���壬B��CΪ���壻D�ı�����Һ�����ˮ�м�����У���Һ�ʺ��ɫ��B��C��Ӧʱ�ɹ۲쵽��ɫ���棬����K������ˮ����ɫ��ҺE������֮��ת����ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �Իش�
�Իش�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com