
| A. | 乙烯使溴水、高锰酸钾溶液褪色 | |
| B. | 碘片、氯化铵晶体受热消失 | |
| C. | 二氧化硫和氯气使品红溶液褪色 | |
| D. | 乙醛、葡萄糖与银氨溶液水浴加热反应 |
分析 A.乙烯与溴水发生加成反应,与高锰酸钾发生氧化反应;
B.碘易升华,氯化铵加热分解;
C.二氧化硫与品红化合生成无色物质,氯气与水反应生成的HClO具有漂白性;
D.乙醛、葡萄糖均含-CHO,均能发生银镜反应.
解答 解:A.乙烯与溴水发生加成反应,与高锰酸钾发生氧化反应,分别发生加成反应、氧化反应,原理不同,故A不选;
B.碘易升华,氯化铵加热分解,分别发生物理变化、化学变化,原理不同,故B不选;
C.二氧化硫与品红化合生成无色物质,氯气与水反应生成的HClO具有漂白性,分别利用化合反应、强氧化性漂白,故C不选;
D.乙醛、葡萄糖均含-CHO,均能发生银镜反应,原理相同,故D选;
故选D.
点评 本题考查物质的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
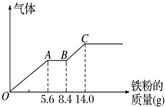 硝酸铜是重要的化工原料,以下三种方法均可得到硝酸铜.
硝酸铜是重要的化工原料,以下三种方法均可得到硝酸铜.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | TiCl4既是氧化产物又是还原产物 | |
| B. | 氧化剂与还原剂的物质的量之比为1:1 | |
| C. | 当转移电子数目为0.2NA时,气体体积增大1.12L | |
| D. | 当有26g固体参加反应时,转移电子数目为NA. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酒精清洗做过碘升华的烧杯 | |
| B. | 用水清洗做过银镜反应的试管 | |
| C. | 用浓盐酸清洗做过高锰酸钾分解实验的试管 | |
| D. | 用氢氧化钠溶液清洗盛过苯酚的试管 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
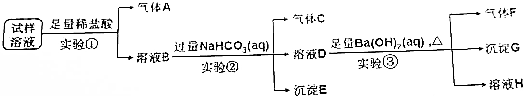
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
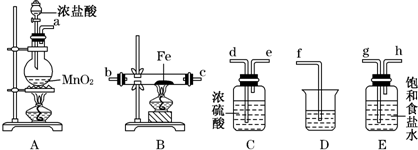
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
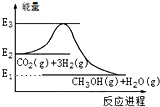
| A. | E2_E1是该反应的热效应 | |
| B. | E3_E1是该反应的热效应 | |
| C. | 该反应放热,在常温常压下就能进行 | |
| D. | 实现变废为宝,且有效控制温室效应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com