

分析 由实验流程可知,含碘废液与亚硫酸钠发生SO32-+I2+H2O=2I-+2H++SO42-,反应后与CCl4分层,分液可分离出CCl4,再通入氯气发生Cl2+2I-=I2+2Cl-,富集、萃取、分液、蒸馏可得到碘,以此来解答.
解答 解:由实验流程可知,含碘废液与亚硫酸钠发生SO32-+I2+H2O=2I-+2H++SO42-,反应后与CCl4分层,分液可分离出CCl4,再通入氯气发生Cl2+2I-=I2+2Cl-,富集、萃取、分液、蒸馏可得到碘,
(1)Na2SO3溶液在空气中存放,容易被氧化成Na2SO4,检验是否存在该杂质的方法是取少量溶液,加入过量稀盐酸,再加入BaCl2溶液,若有白色沉淀生成,则说明含有Na2SO4,
故答案为:Na2SO4;取少量溶液,加入过量稀盐酸,再加入BaCl2溶液,若有白色沉淀生成,则说明含有Na2SO4;
(2)由上述分析可知,操作X为分液,故答案为:分液;
(3)通入Cl2发生反应的离子方程式为Cl2+2I-=I2+2Cl-,故答案为:Cl2+2I-=I2+2Cl-;
(4)含碘废液中加入稍过量的Na2SO3溶液,Na2SO3将废液中的I2还原为I-,这样做的目的是使CCl4中的碘进入水层,从而与CCl4分层,便于分离,
故答案为:使CCl4中的碘进入水层.
点评 本题考查混合物分离提纯,为高频考点,把握分离流程中的反应、混合物分离方法等为解答的关键,侧重分析与实验能力的考查,注意氧化还原反应、分液法应用等,题目难度不大.


科目:高中化学 来源: 题型:推断题
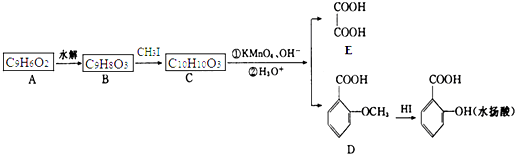
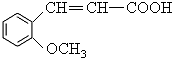 .
.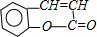 +H2O$\stackrel{酸}{→}$
+H2O$\stackrel{酸}{→}$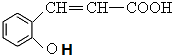 .
.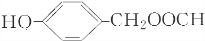 、
、 .
.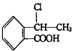 合成
合成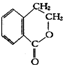
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)>c(CO32-)>c(HCO3-)>c(H2CO3) | B. | c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] | ||
| C. | c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) | D. | c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
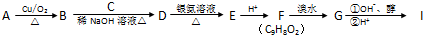

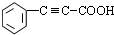 .
.
 、
、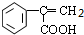 .
. 的合成路线,其它无机试剂任选.
的合成路线,其它无机试剂任选.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光导纤维是以二氧化硅为主要原料制成的 | |
| B. | 在西部和沿海地区兴建风力发电站,解决能源短缺问题 | |
| C. | 糖类、油脂、蛋白质都属于天然有机高分子化合物 | |
| D. | 铁质器具表面刷漆或将其置于干燥处保存,均能有效减缓铁的锈蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 计算机芯片的主要成分是二氧化硅 | |
| B. | 碘盐能防治碘缺乏病,但必须科学合理摄入 | |
| C. | 用电镀废水直接灌溉农田,可提高水资源的利用率 | |
| D. | CO2是导致酸雨发生的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 50 mL该H2SO4中加入足量的铜片并加热,被还原的H2SO4的物质的量为0.46 mol | |
| B. | 稀释该硫酸时应把水倒入硫酸中,边倒边搅拌 | |
| C. | 该硫酸试剂的物质的量浓度为18.4 mol/L | |
| D. | 标准状况下2.7g Al与足量的该硫酸反应可得到H2 3.36L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用a趁热过滤提纯苯甲酸 | B. | 用b制备并检验乙烯 | ||
| C. | 用c分离溴苯与二溴苯混合物 | D. | 用d分离硝基苯与水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
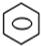 +HNO3(浓)$→_{50℃-60℃}^{浓硫酸}$
+HNO3(浓)$→_{50℃-60℃}^{浓硫酸}$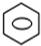 -NO2+H2O;取代反应
-NO2+H2O;取代反应查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com