
| A、硫酸铝溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ |
| B、碳酸钠溶液中加入澄清石灰水:Ca(OH)2+CO32-═CaCO3↓+2OH- |
| C、向碳酸镁悬浊液中加入稀盐酸:CO32-+2H+═CO2↑+H2O |
| D、稀硫酸中加入铁粉:Fe+2H+═Fe2++H2↑ |


科目:高中化学 来源: 题型:
 四种短周期元素A、B、C、D的原子序数依次递增.其中A、B、C三种种元素基态原子的2p能级上都有未成对电子.且未成对电子个数分别是2、3、2;D与C可以形成D2C和D2C2两种化合物.回答下列问题:
四种短周期元素A、B、C、D的原子序数依次递增.其中A、B、C三种种元素基态原子的2p能级上都有未成对电子.且未成对电子个数分别是2、3、2;D与C可以形成D2C和D2C2两种化合物.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2c(H2CO3)+c(HCO3-)+c(H+)═c(OH-) |
| B、c(Na+)═c(HCO3-)+c(H2CO3)+2c(CO32-) |
| C、c(Na+)>c(H+)>c(OH-)>c(CO32-) |
| D、c(Na+)+c(H+)═c(HCO3-)+c(OH-)+2c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化亚铁加入稀硝酸:FeO+2H+=Fe2++H2O |
| B、铝片加入烧碱溶液:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
| C、碳酸氢铵溶液和足量氢氧化钠溶液混合:HCO3-+OH-=CO32-+H2O |
| D、硅酸钠溶液和稀硫酸混合:Na2SiO3+2H+=H2SiO3↓+2Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 利用此图装置可从氯化铁溶液中直接蒸发结晶获得氯化铁晶体 |
B、 利用此图装置可分离石油,得到汽油、煤油和柴油等各种馏分 |
C、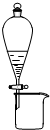 利用此图装置可分离CH3CH2OH和CH3COOC2H5混合液 |
D、 利用此图装置可进行酸碱中和滴定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NA个N2与0.5NA个H2物质的量之比为2:1 |
| B、标准状况下,11.2LBr2含有的原子数为NA |
| C、5.6L氯气和16.8L氧气的混合气体中所含的分子数一定为NA |
| D、1mol/LNaCl溶液中含有NA个氯离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将洁净的三种金属片X、Y和Z分别放置在浸有食盐溶液的滤纸上并压紧(如图).每次实验时,电压表指针的偏移方向和读数如下表.已知构成两电极的金属,活泼性相差越大,则电压越大.对X、Y、Z和铜四种金属的下列说法,不正确的是( )
将洁净的三种金属片X、Y和Z分别放置在浸有食盐溶液的滤纸上并压紧(如图).每次实验时,电压表指针的偏移方向和读数如下表.已知构成两电极的金属,活泼性相差越大,则电压越大.对X、Y、Z和铜四种金属的下列说法,不正确的是( )| 金属片 | 电子流向 | 电压(V) |
| X | X→Cu | +0.78 |
| Y | Cu→Y | -0.15 |
| Z | Z→Cu | +1.35 |
| A、Z金属可作为牺牲阳极保护法的阳极,保护Y金属 |
| B、Y金属不能从硫酸溶液中置换出氢气 |
| C、三种金属的活泼性顺序为:Z>X>Y |
| D、X和Y能构成电压最大的原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、铝粉投入到NaOH溶液中:2Al+2OH-═2Al
| ||
| B、铁与盐酸反应:Fe+2H+═Fe3++H2↑ | ||
C、用小苏打治疗胃酸过多:H++HC
| ||
| D、硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com