
Na、Fe、Cu、Al是常见的金属元素,请按要求回答下列问题:
(1)一定条件下,2.3 g的Na与O2完全反应生成3.6 g产物时失去的电子数为________。
(2)向氯化铜溶液中加入一定量的铁粉和铝粉混合物,充分反应后,下列情况可能出现的是________(填字母)。
a.溶液中有Cu2+、Fe2+、Al3+,不溶物为Cu
b.溶液中有Fe2+、Al3+,不溶物为Cu、Fe
c.溶液中有Fe3+、Al3+,不溶物为Cu
d.溶液中有Fe2+,不溶物为Cu、Al
(3)将一定质量的铁、铝、铜合金,加入1 L一定物质的量浓度的硝酸中,合金完全溶解,测得溶液中(忽略溶液体积的变化)c(H+)=0.5 mol·L-1,c(Cu2+)=0.3 mol·L-1,c(Al3+)=0.2 mol·L-1,c(NO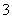 )=2 mol·L-1,则混合物中铁的质量最少为________。
)=2 mol·L-1,则混合物中铁的质量最少为________。
(4)铁的某种氧化物的化学式表示为FexO(x<1),已知铁元素在该氧化物中的质量分数为75%,则x=______(精确至0.01)。
(5)Na—Al/FeS是一种可充电电池,电池中用含Na+导电固体作为电解质,在工作过程中Na+的物质的量保持不变。
①若该正极的电极反应式表示为2Na++FeS+2e-===Na2S+Fe,则电池的负极反应式可表示为________________;充电时,阳极发生反应的物质是________。
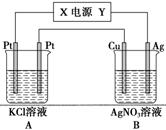
②用该电池作电源,组成如图所示装置,若通电5 min时,铜电极质量增加1.08 g,则该电源电极X名称为________。图中装置A、B的pH变化为A__________、B________(填“增大”、“减小”或“不变”)。
答案 (1)6.02×1022(或0.1NA) (2)ab
(3)5.6 g (4)0.86
(5)①2Na-2e-===2Na+ Na2S、Fe
②负极 增大 不变
解析 (1)钠与氧气完全反应,不论生成Na2O还是Na2O2,钠的化合价均变为+1价,2.3 g钠为0.1 mol,转移电子为0.1 mol。
(2)c中Cu与Fe3+不能大量共存;d中Al与Fe2+不能大量共存。
(3)当合金中的铁生成Fe3+时,其质量最小,根据溶液的电中性可得:c(H+)+2c(Cu2+)+3c(Al3+)+3c(Fe3+)=c(NO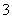 ),代入数据解得c(Fe3+)=0.1 mol,故合金中含有铁0.1 mol,其质量为5.6 g。
),代入数据解得c(Fe3+)=0.1 mol,故合金中含有铁0.1 mol,其质量为5.6 g。
(4)根据题意: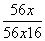 =75%,解得x=0.86。
=75%,解得x=0.86。
(5)①钠为活泼金属,故负极反应应为钠失电子生成Na+。充电时阳极反应为放电时正极反应的逆反应,由放电时正极反应式可知充电时阳极反应物为Na2S、Fe。②由铜电极质量增加1.08 g可知铜电极为阴极,则银电极为阳极,Y为正极,X为负极。A池为电解KCl溶液,pH增大,而B池为电镀池,其pH基本不变。


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
在一密闭容器中,反应mM(气) 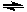 nN(气)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,M的浓度为原来的80%,则( )
nN(气)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,M的浓度为原来的80%,则( )
A、平衡正向移动; B、物质M的转化率增大; C、n > m D、物质N的质量分数减少
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有如下离子组中的若干种:K+、Mg2+、Fe3+、Fe2+、
CO32-、NO3-、SO42-、I-、SiO32-、Cl-且物质的量浓度相同。某同学欲探究该溶液的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到浅紫色火焰;
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成;
Ⅲ.取Ⅱ反应后的溶液分置于两支试管中加入BaCl2溶液,有白色沉淀生成,再滴加
KSCN溶液上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下
层出现紫红色。下列说法正确的是
A.原溶液中肯定不含Mg2+、SiO32-
B.步骤Ⅱ中无色气体可能含有CO2,原溶液中可能含有CO32-
C.原溶液由K+、Fe2+、NO3-、I-、SO42-五种离子组成
D.原溶液中一定含有Mg2+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
硫元素有多种化合价,可形成多种化合物。
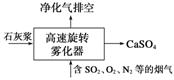
(1)旋转喷雾干燥法是去除燃煤烟气中二氧化硫的方法之一,工艺流程如下图所示,写出雾化器中发生反应的化学方程式:________________________________________________。
(2)已知NaHSO3溶液显弱酸性,其原因用离子方程式表示为____________。
(3)请按照浓度由大到小的顺序排列0.1 mol·L-1 Na2SO3 溶液中的离子________。Na2SO3溶液放置于空气中一段时间后,溶液的pH________(填“增大”、“减小”或“不变”)。
(4)某同学在常温下设计如下实验流程探究Na2S2O3的化学性质。
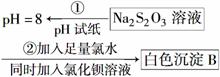
实验①可说明________(填字母)。
A.该Na2S2O3溶液中水电离的c(OH-)=10-8 mol·L-1
B.H2S2O3是一种弱酸
C.Na2S2O3是一种弱电解质
D.Na2S2O3能发生水解,其离子方程式为S2O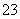 +2H2O===H2S2O3+2OH-
+2H2O===H2S2O3+2OH-
实验②说明Na2S2O3具有________性。写出发生反应的离子方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
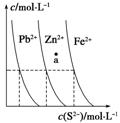 如图为某温度下,PbS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况。下列说法正确的是( )
如图为某温度下,PbS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况。下列说法正确的是( )
A.三种难溶物的溶度积Ksp(FeS)的最小
B.如果向三种沉淀中加盐酸,最先溶解的是PbS
C.向新生成的ZnS浊液中滴入足量含相同浓度的Pb2+、Fe2+的溶液,振荡后,ZnS沉淀会转化为PbS沉淀
D.对于三种难溶物来讲,a点对应的都是不饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)Li3N中氮以N3-存在,基态N3-的电子排布式为________。
(2)O=O键的键能为497.3kJ·mol-1,O—O键的键能为142kJ·mol-1,说明O2中的________键更稳定(填“σ”或“π”)。
(3)BF3与F-可形成BF4-离子。BF3与F-形成BF4-离子时,二者形成的化学键为________键。
(4)X+中所有电子正好充满K、L、M三个电子层,则X的元素符号是________,基态X+的电子排布式为_____________________________________________。
(5)与N2互为等电子体的一种分子为 (填化学式),该分子中σ键与π键的个数比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学小组在实验室中利用CaSO4、NH3、CO2制备(NH4)2SO4,工艺流程如下。
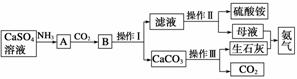
回答下列问题:
(1)操作Ⅰ的名称________,操作Ⅱ需要用到的仪器有铁架台(带铁圈)、酒精灯、玻璃棒和________。
(2)所得母液显酸性的原因用离子方程式表示为______________。检验该溶液含有铵根离子的方法是____________________________。
(3)下列装置能用于实验室制氨气的是________(填序号)。
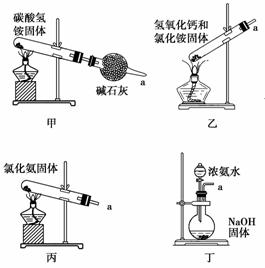
选择氨气的制取装置后,再选用下列装置收集干燥的氨气,并制取硫酸铵溶液,连接的顺序(用接口序号字母表示)是:a接__________________________。
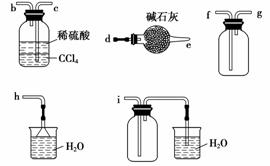
(4)该小组还通过实验研究氨气的性质。
利用下图所示装置探究NH3能否被NO2氧化(K1、K2为止水夹,夹持固定装置略去)。
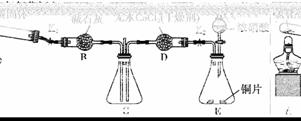
E装置中制取NO2反应的离子方程式是____________。A中发生反应的化学方程式为__________________。
若NH3能被NO2氧化全部生成无毒物质,预期观察到C装置中的现象是____________。若此反应转移电子0.4 mol,则消耗标准状况下的NO2________ L。
实验过程中,未能观察到C装置中的预期现象。该小组同学从反应原理的角度分析了原因,认为可能是:
①NO2氧化性较弱,不能将NH3氧化;
②在此条件下,NH3的转化率极低;
③________________________________________________________________________。
此实验装置存在一个明显的缺陷是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com