
【题目】Co、Ni的化合物在生产生活中有着广泛的应用。
(1)Co元素在周期表中的位置是4周期________族。基态Co原子的简化电子排布式为_________。
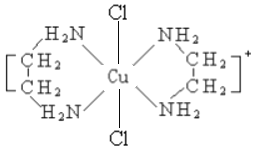
(2)乙二胺NH2-CH2-CH2-NH2(缩写符号en)中N原子的杂化方式为________杂化。en可以与Co形成配合物[Co(en)2Cl2]Cl·HCl·2H2O,配离子结构如下左图所示,中心离子的配位数为_______,配合物晶体中可能存在的作用力有___________。
A 离子键 B 极性共价键 C 非极性共价键 D 配位键 E 氢键
(3)天然氧化镍晶体中总是存在晶体缺陷,如图所示。NiXO晶体中x值为![]() ,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为______。
,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为______。
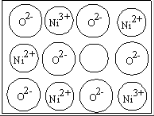
(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列, Ni2+填充其中(如图),己知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为_____g(用a、NA表示)。

【答案】VIII [Ar]3d74s2 sp3 6 ABCDE 8:3 ![]()
【解析】
(1)钴为27号元素,据此书写基态Co原子电子排布式并判断在元素周期表中的位置;
(2)根据杂化轨道数=共价键数+孤电子对数分析判断N原子的杂化类型;根据配离子的结构图判断配位数;该配合物晶体属于离子化合物,结合配体为乙二胺和氯原子分析判断可能存在的作用力;
(3)根据NiXO中化合价代数和为零列式计算;
(4)根据 ,计算含有的原子数,结合小平行四边形的面积计算。
,计算含有的原子数,结合小平行四边形的面积计算。
(1)钴为27号元素,基态Co原子的价电子为其3d、4s能级上的电子,其简化电子排布式为[Ar]3d74s2,位于元素周期表的第四周期Ⅷ族,故答案为:Ⅷ;[Ar]3d74s2;
(2)乙二胺分子中N原子成键时,形成三根共价键,本身含有一对孤电子对,杂化轨道数=共价键数+孤电子对数,则N原子的杂化轨道数目为4,根据杂化轨道理论,N原子为sp3杂化;根据配离子的结构图,该配离子与2个乙二胺分子中的4个N原子形成4个配位键,与2个氯原子形成2个配位键,配位数为6;该配合物晶体属于离子化合物,含有离子键,有机配体中含有共价键,N和C之间是极性键,C与C之间是非极性键,中心原子与配离子间存在配位键,乙二胺分子间还可能形成氢键,故答案为:sp3;6;ABCDE;
(3)设晶体中Ni2﹢与Ni3﹢的最简整数比为x∶y,根据NiXO中化合价代数和为零可知![]() ×0.88=2,由此解得x∶y=8∶3,故答案为:8∶3;
×0.88=2,由此解得x∶y=8∶3,故答案为:8∶3;
(4)根据图知,每个Ni原子被3个O原子包围、每个O原子被3个Ni原子包围,如图 所示,相邻的3个圆中心连线为正三角形,三角形的边长为2apm,每个三角形含有一个Ni原子,含有的O原子数=
所示,相邻的3个圆中心连线为正三角形,三角形的边长为2apm,每个三角形含有一个Ni原子,含有的O原子数=![]() ×3=
×3=![]() ,三角形的面积=[
,三角形的面积=[![]() ×2a×2a×sin60°×10-24]m2=
×2a×2a×sin60°×10-24]m2=![]() ×10-24 a2 m2,如图
×10-24 a2 m2,如图 实际上每个Ni原子被两个小三角形包含,小平行四边形面积为2
实际上每个Ni原子被两个小三角形包含,小平行四边形面积为2![]() ×10-24 a2m2,O原子个数=
×10-24 a2m2,O原子个数=![]() ×2=1,每平方米面积上分散的该晶体的质量=
×2=1,每平方米面积上分散的该晶体的质量=![]() ×
×![]() g=
g=![]() g=
g=![]() g,故答案为:
g,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】柳胺酚是一种药物,其常用的合成路线如下。回答下列问题:
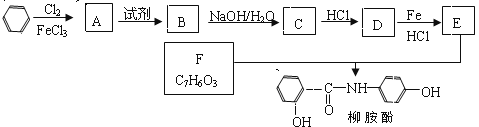

已知:
(1)柳胺酚的化学式为 。
(2)A → B反应所需的试剂是 ; B→ C反应的化学方程式为 。
(3)D→E反应的有机反应类型是 ;物质E含有官能团的名称是 。
(4)E和F反应的化学方程式为 。
(5)写出同时符合下列条件的F的同分异构体的结构简式: 。
①含有苯环;②能发生银镜反应,不能发生水解反应;③在稀NaOH溶液中,1mol该同分异构体能与2molNaOH发生反应;④苯环上有二种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.相同质量的D2O和H2O含有的电子数之比为9:10
B.![]() 和
和![]() 、石墨和金刚石均互为同位素
、石墨和金刚石均互为同位素
C.![]() 、
、![]() 、
、![]() 和H2是氢元素的四种不同粒子
和H2是氢元素的四种不同粒子
D.12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是
A.0.5 mol雄黄( As4S4,结构为![]() )中含有NA个S-S键
)中含有NA个S-S键
B.在1mol /L的NH4NO3溶液滴加氨水使溶液呈中性,则1L该溶液中NH4+的数目为NA
C.标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5NA
D.常温下,将1 mol CH4与1 mol Cl2混合光照,使其充分反应后,生成气体的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池已用于航天飞机,其工作原理如图所示。关于该燃料电池的说法不正确的是
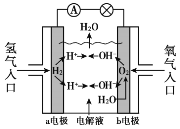
A. H2在负极发生氧化反应
B. 电子从a电极经外电路流向b电极
C. 供电时的总反应为:2H2 + O2 == 2H2O
D. 燃料电池的能量转化率可达100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种新型药物,具有血管扩张活性的选择性β1肾上腺素受体拮抗剂,用于合成该药物的中间体G的部分流程如下:
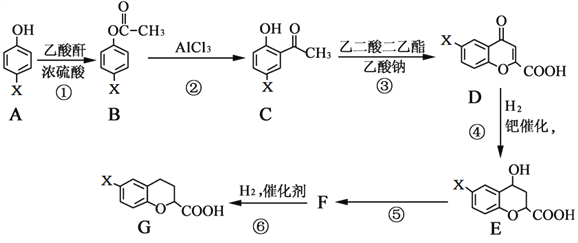
已知:乙酸酐的结构简式为:![]()
请回答下列问题:
(1)G物质中的含氧官能团的名称是________、________。
(2)反应A→B的化学方程式为_________________________________________。
(3)上述④、⑤变化过程的反应类型分别是_______________、______________。
(4)有机物F的结构简式为______________________。
(5)写出满足下列条件的C的同分异构体的结构简式:___________、___________。
Ⅰ. 苯环上只有两种取代基。
Ⅱ. 分子中只有4种不同化学环境的氢。
Ⅲ. 能与NaHCO3反应生成CO2。
(6)根据已有知识并结合相关信息,补充完成以![]() 和乙酸酐为原料制备
和乙酸酐为原料制备![]() 的合成路线流程图(无机试剂任选)。部分合成路线流程图如下:
的合成路线流程图(无机试剂任选)。部分合成路线流程图如下:

请完成合成路线_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要有机化工原料。结合以下路线回答:
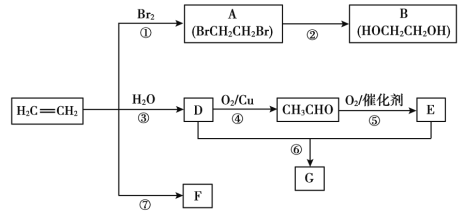
已知:2CH3CHO + O2催化剂,加热2CH3COOH
(1)反应①的化学方程式是_______。
(2)B的官能团是_______。
(3)F是一种高分子,可用于制作食品袋,其结构简式为_______。
(4)G是一种油状、有香味的物质,有以下两种制法。
制法一:实验室用D和E反应制取G,装置如图所示。

i.反应⑥的化学方程式是______,反应类型是_____。
ii.分离出试管乙中油状液体用到的主要仪器是_______。
制法二:工业上用CH2=CH2和E直接反应获得G。
iii.反应类型是___。
iv.与制法一相比,制法二的优点是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸甲酯是调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,用于肥皂、洗涤剂、风味剂和糕点的调味,在医药工业中作为有机合成的中间体.合成肉桂酸甲酯的工业流程如下图所示:

已知:I.醛与醛能发生反应,原理如下:
![]()
Ⅱ.烃A在标准状况下的密度为1.25 g/L.
请回答:
(1)化合物H中的官能团为_____________________________。
(2)肉桂酸甲酯的结构简式为__________________,J的结构简式为________________。
(3)G→H的反应类型为______________________。
(4)写出反应H发生银镜反应的化学方程式_______________,H→I的反应________________(填“能”或“不能”)改用酸性高锰酸钾溶液,简述理由_______________________________________。
(5)符合下列条件的I的同分异构体共有5种。写出另两种同分异构体的结构简式:
A.能发生水解反应
B.与银氨溶液作用出现光亮的银镜
C.能与溴发生加成
 、_____________、_____________。
、_____________、_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关离子晶体的数据大小比较不正确的是( )
A. 晶格能:NaF>NaCl>NaBr
B. 硬度:MgO>CaO>BaO
C. 熔点:NaF>MgF2>AlF3
D. 阴离子的配位数:CsCl>NaCl>CaF2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com