
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.075 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +5,—3 | +3 | +6,—2 | —1 | —2 |
 2AE2(g)已达到平衡状态的是 (填代号)
2AE2(g)已达到平衡状态的是 (填代号)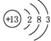 (2分)
(2分)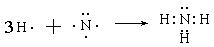 (2分)
(2分) 。
。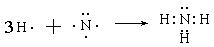 。
。

科目:高中化学 来源:不详 题型:单选题


| A.作为催化剂的材料 | B.电子工业上的半导体材料 |
| C.制造农药的材料 | D.制造耐高温材料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:Na>Si>Cl | B.还原性:Na>Mg>Al |
| C.稳定性:SiH4 >H2S >HCl | D.酸性:H3PO4<H2SO4<HClO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性:HClO4>H3PO4>H2SO4 |
| B.稳定性:SiH4<CH4<NH3 |
| C.碱性:NaOH<KOH<RbOH |
| D.沸点:HF>HI>HBr>HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.所有的物质中都存在化学键 |
| B.原子的次外层电子数都是8 |
| C.稀有气体原子的最外层电子数均为8 |
| D.原子的最外层电子数不超过8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com