
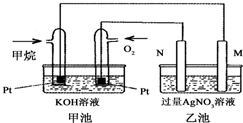
 ��ͼ��һ������ȼ�ϵ�ع���ʱ��ʾ��ͼ���ҳ��е������缫һ����ʯī�缫��һ�������缫������ʱN�缫���������٣���ش��������⣺
��ͼ��һ������ȼ�ϵ�ع���ʱ��ʾ��ͼ���ҳ��е������缫һ����ʯī�缫��һ�������缫������ʱN�缫���������٣���ش��������⣺���� ��1�������Ҵ����Ϊԭ��أ�ͨ�����ĵ缫�Ǹ�����ͨ�������ĵ缫���������ҳ�����ӵ�Դ�����ڵ��أ�����ͼƬ֪������ʱN�缫���������٣�����N���������缫��M����������ʯī�缫������ȼ�ϵ�غ͵��صĹ���ԭ���ش�
��2��ȼ�ϵ�صĸ�������ȼ�Ϸ���ʧ���ӵ�������Ӧ��
��3�������������Һʱ��������ӦʽΪAg++e-=Ag��������ӦʽΪ4OH--4e-=O2��+2H2O����ϵ��ӵ�ת�Ƶ����ʵ������жϽ��м��㣮
��� �⣺��1�������Ҵ����Ϊԭ��أ�ͨ���Ҵ��ĵ缫�Ǹ�����ͨ�������ĵ缫���������ҳ�����ӵ�Դ�����ڵ��أ�����ͼƬ֪������ʱN�缫���������٣�����N���������缫���缫��ӦΪ��Fe-2e-�TFe2+��M����������ʯī�缫��������Ӧ��Ag++e-��Ag��
�ʴ�Ϊ��ʯī��Ag++e-��Ag�� ������ Fe-2e-�TFe2+��
��2��������ȼ�ϵ�صĸ���������ʧ���ӵ�������Ӧ�����Ի����£��缫��ӦʽΪ��CH4-8e-+10OH-=CO32-+7H2O��
�ʴ�Ϊ��CH4-8e-+10OH-=CO32-+7H2O��
��3��n��Ag��=$\frac{4.32g}{108g/mol}$=0.04mol������Ag++e-=Ag��֪ת�Ƶ���Ϊ0.04mol���׳���ͨ��������һ��Ϊ��������ӦʽΪ2O2+8H++8e-=4H2O��������n��O2��=$\frac{1}{4}$��0.04mol=0.01mol��V��O2��=0.01mol��22.4L/mol=0.224L��
�ʴ�Ϊ��0.224��
���� ���⿼����ԭ���ԭ���͵���ԭ������ȷԭ��غ͵��ص缫�Ϸ�����Ӧ�����ͼ��ɷ�������⣬�ѶȲ���ע��缫��Ӧʽ����д��������Һ��������йأ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4Q1+0.5Q2 | B�� | 4Q1+Q2+10Q3 | C�� | 4Q1+2Q2 | D�� | 4Q1+0.5Q2+9Q3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��NH3��=0.010mol/��L��s�� | B�� | v��O2��=0.010mol/��L��s�� | ||
| C�� | v��NO��=0.0010mol/��L��s�� | D�� | v��H2O��=0.045mol/��L��s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
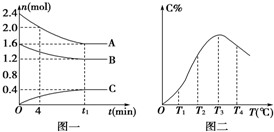 ��10L�ܱ������У�A��B��C������̬���ʹ����˿��淴Ӧ��ϵ��ij�¶�ʱ��A��B��C���ʵ�����ʱ��Ĺ�ϵ��ͼһ��C�İٷֺ������¶ȵĹ�ϵ��ͼ�������з�����ȷ���ǣ�������
��10L�ܱ������У�A��B��C������̬���ʹ����˿��淴Ӧ��ϵ��ij�¶�ʱ��A��B��C���ʵ�����ʱ��Ĺ�ϵ��ͼһ��C�İٷֺ������¶ȵĹ�ϵ��ͼ�������з�����ȷ���ǣ�������| A�� | 0��4 minʱ��A��ƽ����Ӧ����Ϊ0.1 mol/��L•min�� | |
| B�� | �÷�Ӧ��һ�����ȷ�Ӧ | |
| C�� | ƽ��������¶ȣ�Kֵ���� | |
| D�� | �÷�Ӧ��ƽ�ⳣ������ʽΪ��K=$\frac{c��C��}{{c}^{2}��A��c��B��}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������������� | B�� | ������������ʵ���֮��Ϊ16��2��1 | ||
| C�� | ��������ѹǿ��Ϊ16��2��1 | D�� | �������������Ϊ1��8��16 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+ | B�� | H+ | C�� | CO32- | D�� | Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 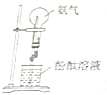 �γɺ�ɫ��Ȫ | B�� | 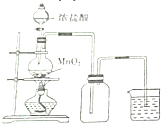 ��ȡ��������������� | ||
| C�� | 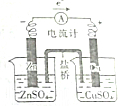 ̽��ԭ���ԭ�� | D�� | 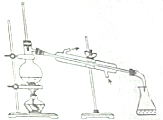 �������ȼ�������Ȼ�̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Na2CO3��NaHCO3����Ba��OH��2��Ca��OH��2��Һ | |
| B�� | ��ȥNa2CO3�����л��е�����NaHCO3���ɲ��ü��ȷ� | |
| C�� | CO2�л�������HCl��SO2������ʱ�����ñ���NaHCO3��Һ�ᴿ���� | |
| D�� | ������ʯ��ˮ����NaHCO3��Һ�У���ʼʱ������Ӧ�����ӷ���ʽΪ��Ca2++2OH-+2HCO3-�TCaCO3��+CO32-+2H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com