
下列有关化学用语使用正确的是( )
 A.乙烯的结构简式:CH2CH2
A.乙烯的结构简式:CH2CH2
B.对氯甲苯的结构简式: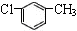
C.CH2ClCH2Cl的名称:二氯乙烷
D.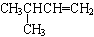 的名称:3-甲基-1-丁烯
的名称:3-甲基-1-丁烯
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年山东省高一下学科竞赛化学试卷(解析版) 题型:选择题
将4.34 g Na、Na2O、Na2O2的混合物与足量水反应,在标准状况下得到672 mL混合气体,将该混合气体点燃,恰好完全反应,则原固体混合物中Na、Na2O、Na2O2的物质的量之比为( )
A.1∶1∶1 B.1∶1∶2
C.1∶2∶1 D.4∶3∶2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下十一次联考化学试卷(解析版) 题型:填空题
观察下列结构简式,回答下列问题:
Ⅰ、乙酸的结构简式为: 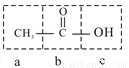
(1)a、c的名称是__________、___________。
(2)b与c组成的原子团的名称是________________。
Ⅱ、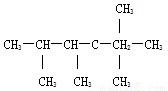
(3)有机物名称是__________________________。
(4)此有机物为烯烃加成的产物,则原来烯烃的结构可能有_______种。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下十一次联考化学试卷(解析版) 题型:选择题
取两份质量相等的有机物M,一份与足量的钠反应放出气体V1升,另一份与足量NaHCO3溶液反应放出气体V2升;若同温同压下V1=V2,则M是 ( )
A.HCOOH
B.HOOC—COOH
C.HOCH2CH2COOH
D.HOC6H4OOCH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下十一次联考化学试卷(解析版) 题型:选择题
把①蔗糖、②淀粉、③蛋白质、④油脂在稀酸存在的条件下分别进行水解,最后只得到一种产物的是
A.①和② B.② C.②③和④ D.④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东济宁微山一中高二下第二次月考化学试卷(解析版) 题型:填空题
氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧的热化学方程式为__________________________________。
(2)氢氧燃料电池能量转化率高,具有广阔的发展前景。现氢氧燃料电池进行下图所示实验:①氢氧燃料电池中,正极的电极反应式为_____ _。
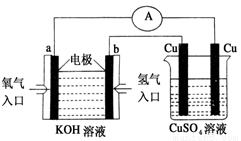
②如图装置中,某一铜电极的质量减轻3.2 g,则a极上消耗的O2在标准状况下的体积为____________L
(3)氢气是合成氨的重要原料,合成氨反应的热化方程式如下:N2(g)+3H2(g) 2NH3(g);ΔH=-92.4 kJ/mol①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),
2NH3(g);ΔH=-92.4 kJ/mol①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),
反应速率与时间的关系如下图所示。

图中t1时引起平衡移动的条件可能是__________其中表示平衡混合物中NH3的含量最高的一段时间是_____
②温度为T ℃时,将2 a mol H2和a mol N2放入0.5 L密闭容器中,充分反应
后测得N2的转化率为50%。则反应的平衡常数为____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东济宁微山一中高二下第二次月考化学试卷(解析版) 题型:选择题
醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是( )
H++CH3COO-,下列叙述不正确的是( )
A.升高温度,平衡正向移动,醋酸的电离常数Ka值增大
B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)增大
C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D.25℃时,欲使醋酸溶液pH、电离常数Ka和电离程度都减小,可加入少量冰醋酸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二6月月考化学试卷(解析版) 题型:选择题
下列实验的结果不能用于说明实验目的的是
代号 | 实验内容 | 实验目的 |
A | Cl2、Br2分别与H2反应 | 比较氯与溴的非金属性强弱 |
B | 向饱和Na2SiO3溶液中通入二氧化碳 | 比较碳与硅的非金属性强弱 |
C | 把碳酸钠与亚硫酸钠放置在空气中 | 比较碳与硫的还原性强弱 |
D | 向氯化铜溶液中加入铁丝 | 比较铁与铜的还原性强弱 |
查看答案和解析>>
科目:高中化学 来源:2017届四川省新高三零诊模拟理综化学试卷(解析版) 题型:填空题
铝硅合金材料性能优良。铝土矿(含 30% SiO2、40.8% Al2O3和少量Fe2O3等)干法制取该合金的工艺如下:
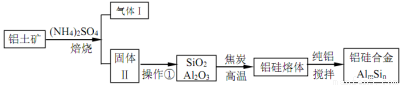
(1)铝硅合金材料中若含铁,会影响其抗腐蚀性。原因是______________。
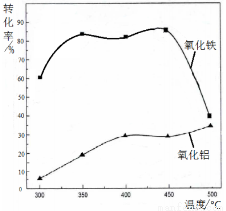
(2)焙烧除铁反应时 Fe2O3 转化为NH4Fe(SO4)2,Al2O3少部分发生类似反应。写出 Fe2O3发生反应的方程式:______________。 氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为______________。
(3)若操作①中所得溶液中加入过量NaOH 溶液,含铝微粒发生反应的离子方程式为:______________。
(4)用焦炭还原SiO2、Al2O3会产生SiC等中间体。写出中间体 SiC 再与Al2O3反应生成铝、硅单质的化学方程式并表出电子转移的方向和数目:______________ 。
(5)已知25℃时Ksp[Al(OH)3]=1.0×10-33,Ksp[Fe(OH)3]=4.0×10-38。向 FeCl3和 AlCl3的混合溶液中逐滴加入NaOH 溶液,生成 Al(OH)3和Fe(OH)3沉淀,当两种沉淀共存时,上层溶液中 c(Al3+):c(Fe3+)=__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com