
分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$结合物质的构成计算该题.
解答 解:等质量的CO和CO2,由n=$\frac{m}{M}$可知,质量相同,物质的量与摩尔质量成反比,即n(CO):n(CO2)=M(CO2):M(CO)=44:28=11:7;
则CO2和CO的碳原子数之比为7:11;
原子数之比为7×3:11×2=21:22;
氧原子的个数之比等于氧原子的物质的量之比,二者含有的氧原子个数之比为:7×2:11×1=14:11;
含氧的质量之比为14:11,
故答案为:7:11;21:22;14:11;14:11.
点评 本题考查了物质的量与各量的计算应用,明确阿伏伽德罗定律及其推论的分析判断和计算是解答的关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
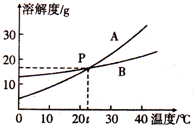 根据图中A、B两种固体物质的溶解度曲线,回答下列问题:
根据图中A、B两种固体物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | FeCl3溶液与Cu粉反应:Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 氯气与水反应:Cl2+H2O?2H++Cl-+ClO- | |
| D. | 氯化铝溶液与过量氨水反应:3NH3•H2O+Al3+=Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,2.24L CO 和O2 混合气体中含有的碳原子数目为0.1NA | |
| B. | 常温常压下,92g NO2和N2O4的混合气体含有的原子数为6NA | |
| C. | 常温常压下,48g O3含有的分子数为3NA | |
| D. | 2.4g金属镁变为镁离子时失去的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体的体积和体系的压强 | B. | 溶液颜色的深浅 | ||
| C. | 固体物质的体积 | D. | H+浓度的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某研究性学习小组设计了一组实验,验证元素周期律.
某研究性学习小组设计了一组实验,验证元素周期律.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com