
(1)小明在做“研究温度对反应速率的影响”实验时,他取了两只试管,均加入4mL 0.01mol/L的KMnO4酸性溶液和2mL 0.1mol/L H2C2O4(乙二酸)溶液,振荡,A试管置于热水中,B试管置于凉水中,记录溶液褪色所需的时间。
①需要用 来酸化KMnO4溶液,褪色所需时间tA tB(填“>”、“=”或“<”).
②写出该反应的离子方程式 .
(2)实验室有瓶混有泥沙的乙二酸样品,小明利用这个反应的原理来测定其含量,具体操作为:
①配制250mL溶液:准确称量5.0g乙二酸样品,配成250mL溶液。
②滴定:准确量取25.00mL所配溶液于锥形瓶中,加少量酸酸化,将0.1000mol?L﹣1KMnO4溶液装入
(填“酸式”或“碱式”)滴定管,进行滴定操作。在实验中发现,刚滴下少量KMnO4溶液时,溶液迅速变成紫红色。将锥形瓶摇动一段时间后,紫红色慢慢消失;再继续滴加时,紫红色就很快褪色了。请解释原因: 。当 ,证明达到滴定终点.
③计算:再重复上述操作2次,记录实验数据如下.
| 序号 | 滴定前读数(mL) | 滴定后读数(mL) |
| 1 | 0.00 | 20.10 |
| 2 | 1.00 | 20.90 |
| 3 | 0.00 | 21.10 |
(1)①硫酸,<;②5H2C2O4+2MnO4﹣+6H+=10CO2↑+2Mn2++8H2O。
(2)②酸式;反应中生成的锰离子具有催化作用,所以随后褪色会加快;当滴入最后一滴高锰酸钾溶液,锥形瓶内的颜色恰好变成紫红色且半分钟不变化;③ 20.00, 90.00% ;④ACD。
解析试题分析:(1)①高锰酸钾具有强氧化性,酸化高锰酸钾溶液应选用非还原性的酸,一般选稀硫酸;当其他条件不变时,温度越高反应速率越快,则褪色时间越短,褪色所需时间tA<tB;②酸性条件下,高锰酸根离子能氧化草酸生成二氧化碳,自身被还原生成锰离子,同时生成水,发生的离子反应方程式为:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O;(2)②酸性高锰酸钾溶液具有强氧化性,只能盛放在酸式滴定管中;在实验中发现,刚滴下少量KMnO4溶液时,溶液迅速变成紫红色。将锥形瓶摇动一段时间后,紫红色慢慢消失;再继续滴加时,紫红色就很快褪色了。原因是高锰酸根离子被还原生成的锰离子有催化作用而导致反应速率加快,当滴入最后一滴高锰酸钾溶液,锥形瓶内的颜色恰好变成紫红色且半分钟不变化,证明达到终点。③分析表中数据知,第3组数据与前两组数据相差较大,应舍去,则消耗KMnO4溶液的平均体积20.00mL;设样品的纯度为x,
5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O
450g 2mol
5.0x×1/10g (0.1×0.020)mol
解得x=90.00%;
④A.未用标准浓度的酸性KMnO4溶液润洗滴定管,会导致酸性高锰酸钾浓度偏小,需要高锰酸钾溶液体积偏大,测定结果偏高,正确;B.滴定前锥形瓶有少量水,对测定结果无影响,错误;C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失,高锰酸钾溶液体积偏大,测定结果偏高,正确;D.不小心将少量酸性KMnO4溶液滴在锥形瓶外,高锰酸钾溶液体积偏大,测定结果偏高,正确;E.观察读数时,滴定前仰视,滴定后俯视,高锰酸钾溶液体积偏小,测定结果偏低,错误;选ACD。
考点:


科目:高中化学 来源: 题型:填空题
白铁皮(镀锌铁皮)常用于制造屋面、卷管和各种容器,利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程如下: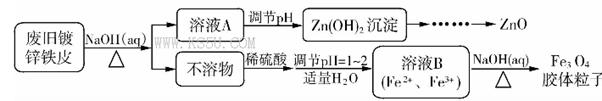
已知:Zn及其化合物的性质与Al及其化合物的性质相似。请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮的作用是____________。
a.去除油污 b.溶解镀锌层 c.去除铁锈 d.钝化
(2)为获得Fe3O4胶体粒子,溶液B中必须含有一定量的Fe2+,可利用________检验其是否存在。
a.NaOH溶液 b.KSCN溶液 c.溶液KMnO4 d.氯水
(3)由溶液B制备Fe3O4胶体粒子的过程中,必须持续通入N2以保证产品的纯度,其原因是_____________ .
(4)在工业上常用水热法制造Fe3O4胶体粒子,有利于提高其纯度和磁性能,主要反应过程为:Fe2++S2O32-+O2+OH- Fe3O4(胶体)+S4O62-+H2O
Fe3O4(胶体)+S4O62-+H2O
①反应过程中起还原剂作用的微粒是________________;
②若反应过程中产生的Fe3O4(胶体)与S4O62-均为1mol,则参加反应的氧气在标准状况下的体积为____________L。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(14分)硒(34Se)和碲(52Te)都是第VIA族元素,硒是分布在地壳中的稀有元素。工业上硒鼓废料(主要成分硒、碲、碳、铜和铁合金)回收精炼硒的流程如下: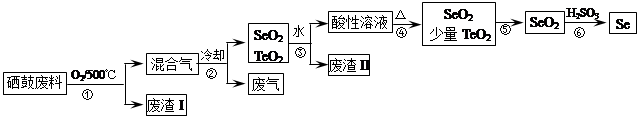
已知:
| 物理性质 | 熔点 | 沸点 | 升华 | 溶解性 |
| SeO2 | 340℃ | 684℃ | 315℃ | 易溶于水 |
| TeO2 | 733℃ | 1260℃ | 450℃ | 微溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
.[实验化学]
苯亚甲基苯乙酮俗称查尔酮,淡黄色棱状晶体,熔点58℃,沸点208℃(3.3kPa)易溶于醚、氯仿和苯,微溶于醇。制备原理如下: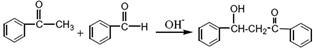
 (查尔酮)
(查尔酮)
(1)制备过程中,需在搅拌下滴加苯甲醛,并控制滴加速度使反应温度维持在25~30℃,说明该反应是 (填放热或吸热)反应。如温度过高时,则可以采取 措施。
(2)产品结晶前,可以加入几粒成品的查尔酮,其作用是 。
(3)结晶完全后,需抽滤收集产物。抽滤装置所包含的仪器除
减压系统外还有 、 (填仪器名称)。
(4)获得的深色粗产品加入活性炭,以95%乙醇重结晶。加入活性炭的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2
相关物质的溶解性见下表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |

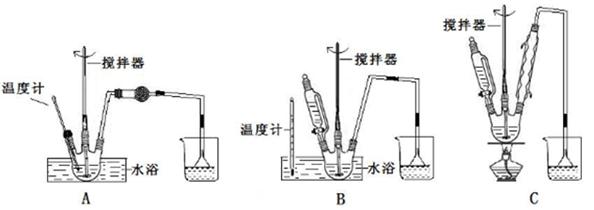
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(16分)某化学兴趣小组在进行钠在空气中燃烧的实验,请写出钠在氧气中燃烧的化学方程式: 。实验后,同学们发现除了得到黄色物质外,产物中还有黑色物质。兴趣小组的同学对产生的黑色固体物质进行实验探究。
查阅资料:
工业上采用铁环作阴极电解得到金属钠。实验室中金属钠的标签主要内容如下: 
提出猜想:
猜想1:钠附着煤油,煤油的不完全燃烧可以生成碳单质;猜想2: 与钠反应也可以生成碳单质;
猜想3: ; 猜想4:……
设计实验方案,验证猜想:
| 实验目的 | 实验步骤 | 实验现象 | 结论 |
| 验证猜想1 | 将一小块钠从煤油中直接取出加热燃烧 取出一小块切去表皮并擦干净煤油的钠加热燃烧 | | 黑色物质中含 有碳单质 |
| 验证猜想3 | | | 黑色物质中 含有铁元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(20分)某研究性学习小组在实验室中配制0.20mol·L-1的盐酸标准溶液,然后用其滴定某未知浓度的氢氧化钠溶液。
⑴配制待测液:将1.7 g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成200 mL溶液,所需的主要玻璃仪器除烧杯,200 mL容量瓶,量筒,还有 ﹑ 。
⑵滴定:
①盛装0.20mol·L-1盐酸标准液应该用 式滴定管,
②滴定时,先向锥型瓶中加酚酞作为指示剂;再逐滴滴定,观察到 时为滴定终点。
③有关数据记录如下:
| 滴定序号 | 待测液体体积(mL) | 所耗盐酸标准液的体积(mL) | |
| 起始读数 滴定前 | 终点读数 | ||
| 1 | 20.00 | 0.50 | 20.40 |
| 2 | 20.00 | 6.00 | 26.10 |
| 3 | 20.00 | 4.00 | 24.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某同学旅游时发现,苗族人的银饰美丽而富有民族文化,制作银饰时可以选用Fe(NO3)3溶液做蚀刻剂。受此启发,该同学所在的化学兴趣小组在实验室选用Fe(NO3)3溶液清洗做过银镜反应的试管,发现不但银镜溶解,而且较少产生刺激性气体。
化学兴趣小组对Fe(NO3)3溶液溶解银的原理进行探究:
【提出假设】假设1: Fe(NO3)3溶液显酸性,在此酸性条件下NO3-能氧化Ag;
假设2:Fe3+具有氧化性,能氧化Ag
【验证假设】
(1)甲同学验证假设1。
①他用淡紫色的Fe(N03)3·9H20晶体(分析纯,Mr=404)配制1.5mol/L的Fe(N03)3落液100mL。需要称取_____g Fe(N03)3·9H20晶体,配制过程中所用到的仪器除烧杯、玻璃棒外还必需:__________
②测得1.5 mol/L的Fe(NO3)3溶液pH约为1,其原因用化学用语表示为____。
③将pH=1的HN03溶液加入到镀有银镜的试管中,振荡,观察到银镜慢慢溶解,产生无色气体并在液面上方变为红棕色,溶液中发生反应的离子方程式应是_____
④将1.5mol/L的Fe(NO3)3溶液加入到镀有银镜的试管中,振荡,观察到银镜很快溶解,并且溶液颜色加深。
(2)乙同学验证假设2。分别用溶质的质量分数为2%、10%的足量FeCl3溶液加入到镀有银镜的试管中,振荡,都看不出银镜溶解。乙同学由此得出结论,假设2不成立。
你是否同意乙的结论?_______,简述理由:_______
【思考与交流】I甲同学的实验④中,溶液颜色为什么会加深?查阅资料得知,Fe2+能与NO形成配离子: (棕色)。已知,同浓度的硝酸氧化性比Fe3+略强。
(棕色)。已知,同浓度的硝酸氧化性比Fe3+略强。
根据以上信息综合分析,浓、稀Fe(N03)3溶液溶解银镜时,发生的反应有何不同?
__________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com