
分析 (1)依据化合价代数和为0计算解答;钒(V)的原子序数为23,位于周期表第四周期ⅤB族;
(2)偏钒酸铵受热分解生成V2O5和氨气、水,依据反应中是否有化合价变化判断是否是氧化还原反应;
(3)工业上常用V2O5跟金属铝粉发生铝热反应得到金属钒,发生铝热反应生成V和氧化铝;
(4)①放电时为原电池,负极发生氧化反应,+2价钒失去电子生成+3价钒;
②电镀池为电解池,阳极为镀层金属,阴极为镀件.
解答 解(1)NH4VO3中铵根离子为+1价,O为-2价,根据化合物代数和为0,计算得V的化合价为+5价;钒(V)的原子序数为23,核外电子排布为1s22s22p63s23p63d34s2,位于周期表第四周期ⅤB族,
故答案为:+5;否;
(2)偏钒酸铵受热分解生成V2O5和氨气、水,反应的化学方程式为2NH4VO3$\frac{\underline{\;\;△\;\;}}{\;}$V2O5+2NH3+H2O,元素化合价没有发生变化,不是氧化还原反应,
故答案为:2NH4VO3$\frac{\underline{\;\;△\;\;}}{\;}$V2O5+2NH3+H2O;非氧化还原反应;
(3)工业上常用V2O5跟金属铝粉发生铝热反应得到金属钒,发生铝热反应生成V和氧化铝,反应的方程式为3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$6V+5Al2O3,反应中V的化合价由+5价降低到0价,则每生成1molV,转移的电子的物质的量为5mol,
故答案为:3V2O5+10Al $\frac{\underline{\;高温\;}}{\;}$6V+5Al2O3;5;
(4)①放电时为原电池,负极发生氧化反应,+2价钒失去电子生成+3价钒,电极反应式:V2+-e-=V3+;
②电镀池为电解池,阳极为镀层金属,阴极为镀件,铁制品上镀铜铁制品应与电池的负极相连为电解池的阴极;
故答案为:V2+-e-=V3+;负极.
点评 本题考查了金属的冶炼与原电池、电解池知识,明确铝热反应原理及原电池、电解池工作原理是解题关键,侧重于学生的分析能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
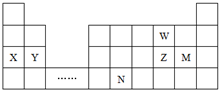
| A. | 原子半径:Y>Z>W | |
| B. | 单质的还原性:X>Y | |
| C. | 溴与元素M同主族,最高价氧化物的水化物的酸性比M的强 | |
| D. | 元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室里易燃试剂与强氧化性试剂应分开放置并远离火源 | |
| B. | 在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 | |
| C. | 滴定实验中所用到的滴定管和移液管,在使用前均需干燥或用相应的溶液润洗,容量瓶、锥形瓶则不应润洗 | |
| D. | 将含有少量氯化钾的硝酸钾放入烧杯中,加水溶解并加热、搅拌,当溶液表面出现一层晶膜时停止加热,冷却结晶,过滤即可得到大量硝酸钾晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
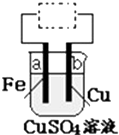 用铁片(电极a)、铜片(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )
用铁片(电极a)、铜片(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )| A. | 构成原电池时b极反应为:Cu-2e-═Cu2+ | |
| B. | 构成的原电池或电解池工作后就可能产生大量气体 | |
| C. | 构成电解池时b 极质量既可能减少也可能增加 | |
| D. | 构成电解池时a极质量一定会减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
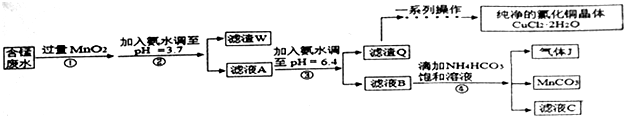
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
| 完全沉淀的pH | 9.7 | 3.7 | 6.4 | 10.4 |
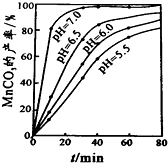
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将5 mL 0.02 mol/L的H2SO4溶液与5 mL 0.02 mol/L NaOH溶液充分混合,若混合后溶液的体积为10 mL,则混合液的pH=2 | |
| B. | 某物质的溶液中由水电离的c(H+)=1×10-a mol/L,若a>7,则pH一定为14-a | |
| C. | pH相等的①CH3COONa ②C6H5ONa ③NaHCO3溶液,c(Na+)大小关系:①>③>② | |
| D. | CH3COONa溶液中加入少量KNO3固体后的碱性溶液一定有:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾净水原理为:Al3++3H2O=Al(OH)3↓+3H+ | |
| B. | 该溶液中AlO2-、F-、K+、Na+能大量共存 | |
| C. | 加入过量NH3•H2O反应的离子方程式为:Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| D. | 加入过量Ba(OH)2溶液反应的离子方程式为:Al3++2SO42-+4OH-+2Ba2+=AlO2-十2BaSO4↓+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com