
��ӦaM(g)��bN(g)cP(g)��dQ(g)�ﵽƽ��ʱ��M���������y(M)�뷴Ӧ�����Ĺ�ϵ��ͼ��ʾ������z��ʾ��Ӧ��ʼʱN�����ʵ�����M�����ʵ���֮�ȡ�����˵����ȷ����(����)
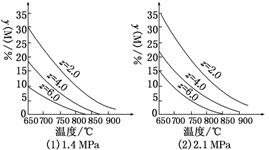
A��ͬ��ͬѹͬzʱ�����������ƽ��ʱQ�������������
B��ͬѹͬzʱ�������¶ȣ�ƽ��ʱQ�������������
C��ͬ��ͬzʱ������ѹǿ��ƽ��ʱQ�������������
D��ͬ��ͬѹʱ������z��ƽ��ʱQ�������������
 �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д� Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й��ڻ�ѧ���������ʶ����ȷ����
A��CaO����SO2��Ӧ��CaO������ҵ�����������
B��ͬŨ�ȵ�Na2CO3��Һ�ڲ�ͬ�¶��µ�ȥ��������ͬ
C��������ɱ�����в�������Ϊ�����ĵ��������ȱ���
D������ˮ��ʱ�������������ԵĽ������ӣ�����Ư��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������10mL pH=3�Ĵ�����Һ�м���ˮϡ�ͺ�����˵����ȷ���� ( )
A����Һ�е������ӵ���Ŀ���ӣ���������ǿ
B������ĵ���̶�����С
C���ټ���10mL pH=11 NaOH��Һ�����ҺpH=7
D����Һ����ˮ�������=1��10-11 mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ǧ���صĹ���ԭ��Ϊ�� Pb��PbO2��2H2SO4===2PbSO4��2H2O���ж���ͼ�������жϲ���ȷ����(����)
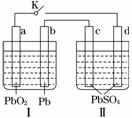
A. K�պ�ʱ��d�缫��Ӧʽ��PbSO4��2H2O��2e��===PbO2��4H����SO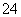
B. ����·��ת��0.2 mol����ʱ���������ĵ�H2SO4Ϊ0.2 mol
C. K�պ�ʱ������SO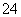 ��c�缫Ǩ��
��c�缫Ǩ��
D. K�պ�һ��ʱ���ɵ�����Ϊԭ��أ�d�缫Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼװ����ʾ��C��D��E��F��X��Y���Ƕ��Ե缫���ס�������Һ�������Ũ�ȶ���ͬ(����ͨ��ǰ����Һ�������)��A��BΪ���ֱ����Դ����������ֱ����Դ��ͨ��F�������ʺ�ɫ��
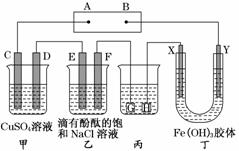
��ش�
(1)B���ǵ�Դ��______________��һ��ʱ�������Һ��ɫ________������X����������ɫ��dz��Y����������ɫ��������_____________________________��
�ڵ糡��������Y���ƶ���
(2)���ס���װ���е�C��D��E��F�缫��ֻ��һ�ֵ�������ʱ����Ӧ���ʵ����ʵ���֮��Ϊ________��
(3)���ñ�װ�ø�ͭ����������HӦ��______________(��Ʋ�������Ƽ���)�����Һ��________��Һ����������Һ��pH��13ʱ (��ʱ����Һ���Ϊ500 mL)�����жƼ���������������Ϊ________��������Һ��pH________(������С�����䡱)��
(4)����C�缫��Ϊ��������װ�ö����䣬����з������ܷ�Ӧ�����ӷ���ʽΪ________________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��ʾ��ʾ���������Ĺ̵���Ӧ����N2��3H22NH3�͢�N2��O22NO��ƽ�ⳣ��(lg K)���¶ȵĹ�ϵ������ͼ�е������ж�����˵����ȷ����(����)
A����Ӧ��Ϊ���ȷ�Ӧ
B�������£���Ӧ�ٵķ�Ӧ���ʺܴ���Ӧ�ڵķ�Ӧ���ʺ�С
C�������¶ȣ���Ӧ�ٵķ�Ӧ��������Ӧ�ڵķ�Ӧ���ʼ�С
D���ڳ����£����÷�Ӧ�ٹ̵������÷�Ӧ�ڹ̵���Ӧ�̶����ܴ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������ĵ���ƽ�ⳣ�����±���
| ������ | HCOOH | ��HCN | H2CO3 |
| ����ƽ�ⳣ��(25 ��) | Ki��1.77��10��4 | Ki��4.9��10��10 | Ki1��4.3��10��7 Ki2��5.6��10��11 |
����ѡ��������(����)
��2CN����H2O��CO2===2HCN��CO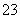
��2HCOOH��CO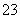 ===2HCOO����H2O��CO2��
===2HCOO����H2O��CO2��
���к͵��������pH��HCOOH��HCN����NaOH����ǰ��С�ں���
�ܵ��������Ũ�ȵ�HCOONa��NaCN��Һ��������������ǰ��С�ں���
A���٢ڡ������������������� B���ڢ�
C���ۢܡ� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
NA���������ӵ�����������˵����ȷ���ǣ���
| A�� | 2.3g����ԭ�ӱ������ʱ���õ��ĵ�����Ϊ0.1NA | |
| B�� | 0.2NA�����������19.6g���Ậ����ͬ����ԭ���� | |
| C�� | 28g���������е�ԭ����ΪNA | |
| D�� | NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
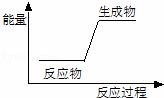 ���з�Ӧǰ�����ʵ��������仯������ͼ��ʾ����
���з�Ӧǰ�����ʵ��������仯������ͼ��ʾ����
A��H��F�TH+F
B��Mg+2H+=Mg2++H2��
C��2Na+2H2O=2Na++2OH-+ H2��
D��HNO3+NaOH=NaNO3+H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com