
ЁОЬтФПЁПвбжЊЖЯПЊ1 mol Cl2(g)жаClЃClМќашвЊЮќЪе243 kJФмСПЁЃИљОнФмСПБфЛЏЪОвтЭМЃЌЯТСаЫЕЗЈЛђШШЛЏбЇЗНГЬЪНе§ШЗЕФЪЧ
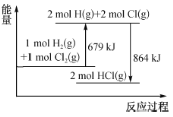
A.H2(g)+Cl2(g)=2HCl(g) ЁїH=Ѓ185 kJЁЄmolЃ1
B.ЩњГЩ1 mol H2(g)жаЕФHЃHМќЗХГі121.5 kJФмСП
C.ЖЯПЊ1 mol HCl(g)жаЕФHЃClМќвЊЮќЪе864 kJФмСП
D.HCl(g)=![]() H2(g)+
H2(g)+![]() Cl2(g) ЁїH=Ѓ92.5 kJЁЄmolЃ1
Cl2(g) ЁїH=Ѓ92.5 kJЁЄmolЃ1
ЁОД№АИЁПA
ЁОНтЮіЁП
A. гЩЭМПЩжЊH2(g)+Cl2(g)=2HCl(g) ЁїH=-(864-679) kJ/mol=-185 kJ/molЃЌAе§ШЗЃЛ
B. гЩЭМПЩжЊЖЯПЊ1 mol H2(g)жаЕФHЃHМќКЭ1 mol Cl2(g)жаЕФClЃClМќашЮќЪе679 kJ/molЕФФмСПЃЌЖјвбжЊЖЯПЊ1 mol Cl2(g)жаClЃClМќашвЊЮќЪе243 kJФмСПЃЌЫљвдЖЯПЊЖЯПЊ1 mol H2(g)жаЕФHЃHМќашвЊЮќЪеЕФФмСПЮЊ679 kJ-243 kJ=436 kJЃЌвђДЫЩњГЩ1 mol H2(g)жаЕФHЃHМќЗХГі436 kJФмСПЃЌBДэЮѓЃЛ
C. ЩњГЩ2 mol HCl (g)жаЕФH-ClМќЗХГі864 kJЕФФмСПЃЌЫљвдЩњГЩ2 mol HCl (g)жаЕФH-ClМќЗХГі432 kJЕФФмСПЃЌдђЖЯПЊ1 mol HCl(g)жаЕФHЃClМќвЊЮќЪе432 kJФмСПЃЌCДэЮѓЃЛ
D. ИљОнбЁЯюAЗжЮіПЩжЊ2 mol HCl(g)ЗДгІВњЩњ1 mol H2(g)КЭ1 mol Cl2(g)ЮќЪе185 kJЕФФмСПЃЌвђДЫ1 mol HClЗДгІВњЩњH2(g)ЁЂCl2(g)ЮќЪе92.5 kJЕФШШСПЃЌШШЛЏбЇЗНГЬЪНЮЊHCl(g)=![]() H2(g)+
H2(g)+![]() Cl2(g) ЁїH=+92.5 kJЁЄmolЃ1ЃЌDДэЮѓЃЛ
Cl2(g) ЁїH=+92.5 kJЁЄmolЃ1ЃЌDДэЮѓЃЛ
ЙЪКЯРэбЁЯюЪЧAЁЃ


 ЬьЬьЯђЩЯвЛБОКУОэЯЕСаД№АИ
ЬьЬьЯђЩЯвЛБОКУОэЯЕСаД№АИ аЁбЇЩњ10ЗжжггІгУЬтЯЕСаД№АИ
аЁбЇЩњ10ЗжжггІгУЬтЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛИіШнЛ§ЮЊ2 LЕФУмБеШнЦїжаЃЌМгШы0.8 molЕФA2ЦјЬхКЭ0.6 mol B2ЦјЬхЃЌвЛЖЈЬѕМўЯТЗЂЩњШчЯТЗДгІЃКA2(g)ЃЋB2(g)![]() 2AB(g)ЁЁІЄH<0ЃЌЗДгІжаИїЮяжЪЕФХЈЖШЫцЪБМфЕФБфЛЏЧщПіШчЭМЫљЪОЃЌЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
2AB(g)ЁЁІЄH<0ЃЌЗДгІжаИїЮяжЪЕФХЈЖШЫцЪБМфЕФБфЛЏЧщПіШчЭМЫљЪОЃЌЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
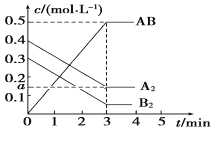
A. ЭМжаaЕуЕФжЕЮЊ0.15 B. ИУЗДгІЕФЦНКтГЃЪ§KЃН0.03
C. ЮТЖШЩ§ИпЃЌЦНКтГЃЪ§KжЕМѕаЁ D. ЦНКтЪБA2ЕФзЊЛЏТЪЮЊ62.5%
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊ1gЧтЦјЭъШЋШМЩеЩњГЩвКЬЌЫЎЪБЗХГіШШСП143kJ,18gЫЎеєЦјБфГЩвКЬЌЫЎЗХГі44kJЕФШШСПЁЃЦфЫћЯрЙиЪ§ОнШчБэ:
O=O | HЁЊH | HЁЊO(g) | |
МќФм/(kJЁЄmol-1) | 496 | 436 | x |
дђБэжаxЮЊ
A.920B.557C.463D.188
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПжјУћЕМбнГТЯўЧфжДЕМЕФМЭТМЦЌЁЖЗчЮЖШЫМфЁЗжаЕквЛМЏжаНщЩмСЫвЛжжДЈЮїЕиЧјЕФУёМфУРЪГ-ЛвЫЎжѓЫёЃЌетРяЕФЁАЛвЫЎЁБМДжИМгСЫВнФОЛвЕФЫЎЁЃВнФОЛвжаИЛКЌK2CO3ЃЈЛЙгаЩйСПЕФKClКЭK2SO4ЃЉЃЌФГаЫШЄаЁзщДђЫуДгЁАЛвЫЎЁБжаЬсШЁKClЃЌЧыФуАяЫћУЧЭъГЩвдЯТЙЄзїЁЃ
(1)МьбщЁАЛвЫЎЁБШмвКжаЕФSO42______________________________________________________________________ЁЃ
(2)МьбщЁАЛвЫЎЁБШмвКжаЕФCO32ЁЃ
ЂйаЁзщФкгаЭЌбЇШЯЮЊЃЌЭљЩЯВуГЮЧхШмвКжаЕЮШыCa(OH)2ШмвКЙлВьАзЩЋГСЕэВњЩњМДПЩжЄУїЦфжаКЌгаCO32ЁЃФуШЯЮЊДЫЗНАИЪЧЗёе§ШЗЃП__________ЃЈЬюЁАе§ШЗЁБЛђЁАДэЮѓЁБЃЉЃЌРэгЩЪЧ__________________________________________________________ЁЃ
ЂкаЁзщФкСэвЛЭЌбЇШЯЮЊЃЌгІЭљГЮЧхШмвКжаМгШыЙ§СПЯЁбЮЫсЃЌЭЈЙ§______ЕФЯжЯѓХаЖЯCO32-ЕФДцдкЁЃаДГіМгШыЙ§СПбЮЫсЗДгІЕФРызгЗНГЬЪН__________________________ЁЃ
(3)ОЙ§ГфЗжЬжТлКѓЃЌаЁзщФкЭЌбЇЙВЭЌЩшМЦГіСЫЯТУцЕФЗжРыЬсДПТЗЯпЃК

ЂйЁАЛьКЯЮя1ЁБОЙ§вЛЯЕСаВйзїзюжеЕУЕНKClЙЬЬхЃЌЯТСаВйзїЫГађКЯРэЕФЪЧ______ЁЃ
aЁЂМгШыЙ§СПK2CO3ШмвК BЁЂМгШыЙ§СПЯЁбЮЫс CЁЂЙ§ТЫ DЁЂеєЗЂНсОЇ
AЁЂaЁњbЁњcЁњd BЁЂaЁњcЁњbЁњd
CЁЂbЁњcЁњaЁњd DЁЂcЁњaЁњbЁњd
ЂкЪЕбщЪвжаЃЌеєЗЂНсОЇВйзїгІдк___________ЃЈЬювЧЦїУћГЦЃЉжаНјааЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП(1)ШчЭМЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПБъЧЉЩЯЕФгаЙиЪ§ОнЃЌИљОнЪ§ОнМЦЫуИУХЈбЮЫсжаHClЕФЮяжЪЕФСПХЈЖШЮЊ____________ЁЃ

(2)ШЁгУШЮвтЬхЛ§ЕФИУбЮЫсШмвКЪБЃЌЯТСаЮяРэСПжаВЛЫцЫљШЁЬхЛ§ЕФЖрЩйЖјБфЛЏЕФЪЧ______ЃЎ
AЃЎШмвКжаHClЕФЮяжЪЕФСП BЃЎШмвКЕФХЈЖШ
CЃЎШмвКжаCl-ЕФЪ§ФП DЃЎШмвКЕФУмЖШ
(3)ФГбЇЩњгћгУЩЯЪіХЈбЮЫсКЭеєСѓЫЎХфжЦ480mLЮяжЪЕФСПХЈЖШЮЊ0.400mol/LЕФЯЁбЮЫсЁЃ
ЂйИУбЇЩњашвЊСПШЁ______mLЩЯЪіХЈбЮЫсНјааХфжЦЃЌШЗЖЈШмвКЬхЛ§ЕФШнЦїЪЧ________ЃЈЬюУћГЦЃЉЁЃ
ЂкдкХфжЦЙ§ГЬжаЃЌЯТСаЪЕбщВйзїЖдЫљХфжЦЕФЯЁбЮЫсЕФЮяжЪЕФСПХЈЖШгаКЮгАЯьЃПЃЈдкРЈКХФкЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЛђЁАЮогАЯьЁБЃЉЁЃ
aЃЎЪЕбщЧАЃЌШнСПЦПжагаЩйСПеєСѓЫЎ.___________ЁЃ
bЃЎгУСПЭВСПШЁХЈбЮЫсЪБИЉЪгЙлВьАМвКУцЃЎ__________ЁЃ
c.ЖЈШнКѓОеёЕДЁЂвЁдШЁЂОВжУЃЌЗЂЯжвКУцЯТНЕЃЌдйМгЪЪСПЕФеєСѓЫЎЃЎ__________ЁЃ
(4)ЂйМйЩшИУЭЌбЇГЩЙІХфжЦСЫ0.400mol/LЕФбЮЫсЃЌЫћгжгУИУбЮЫсжаКЭКЌ0.4gNaOHЕФNaOHШмвКЃЌдђИУЭЌбЇашШЁ______mLбЮЫсЃЎ
ЂкМйЩшИУЭЌбЇгУаТХфжЦЕФбЮЫсжаКЭКЌ0.4gNaOHЕФШмвКЃЌЗЂЯжБШЂйжаЫљЧѓЬхЛ§ЦЋаЁЃЌдђПЩФмЕФдвђЪЧ________________ЁЃ
AЃЎХЈбЮЫсЛгЗЂЃЌХЈЖШВЛзу BЃЎХфжЦШмвКЪБЃЌЮДЯДЕгЩеБ
CЃЎХфжЦШмвКЪБЃЌИЉЪгШнСПЦППЬЖШЯп DЃЎМгЫЎЪБГЌЙ§ПЬЖШЯпЃЌгУНКЭЗЕЮЙмЮќГі
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПXЁЂYЁЂZЁЂMЁЂQЁЂRЪЧ6жжЖЬжмЦкдЊЫиЃЌЦфдзгАыОЖМАжївЊЛЏКЯМлШчЯТЃК
дЊЫиДњКХ | X | Y | Z | M | Q | R |
дзгАыОЖ/nm | 0.160 | 0.143 | 0.102 | 0.075 | 0.077 | 0.037 |
жївЊЛЏКЯМл | ЃЋ2 | ЃЋ3 | ЃЋ6ЃЌЃ2 | ЃЋ5ЃЌЃ3 | ЃЋ4ЃЌЃ4 | ЃЋ1 |
ЃЈ1ЃЉZдкдЊЫижмЦкБэжаЕФЮЛжУЪЧ_________________________ЁЃ
ЃЈ2ЃЉдЊЫиQКЭRаЮГЩЕФЛЏКЯЮяAЪЧЙћЪЕДпЪьМСЃЌгУAжЦБИввДМЕФЛЏбЇЗНГЬЪНЪЧ_______________________ЁЃ
ЃЈ3ЃЉЕЅжЪЭКЭдЊЫиMЕФзюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяЕФХЈШмвКЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ___________________ЁЃ
ЃЈ4ЃЉдЊЫиXЕФН№ЪєадБШдЊЫиY______ЃЈЬюЁАЧПЁБЛђЁАШѕЁБЃЉЁЃ
ЃЈ5ЃЉдЊЫиQЁЂдЊЫиZЕФКЌСПгАЯьИжЬњадФмЃЌВЩгУЯТЭМзАжУAдкИпЮТЯТНЋИжбљжадЊЫиQЁЂдЊЫиZзЊЛЏЮЊQO2ЁЂZO2ЁЃ

ЂйЦјЬхaЕФГЩЗжЪЧ________________ЃЈЬюЛЏбЇЪНЃЉЁЃ
ЂкШєИжбљжадЊЫиZвдFeZЕФаЮЪНДцдкЃЌдкAжаЗДгІЩњГЩZO2КЭЮШЖЈЕФКкЩЋбѕЛЏЮяЃЌдђЗДгІЕФЛЏбЇЗНГЬЪНЪЧ_________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПAЁЂBЁЂCЁЂDЫФжждЊЫиЃЌЫќУЧдзгЕФКЫЕчКЩЪ§ОљаЁгк18ЃЌЧввРДЮЕндіЁЃAдзгКЫФкНіга1ИіжЪзгЃЌBдзгЕФЕчзгзмЪ§гыDдзгЕФзюЭтВуЕчзгЪ§ЯрЕШЃЌAдзггыBдзгЕФзюЭтВуЕчзгЪ§жЎКЭгыCдзгЕФзюЭтВуЕчзгЪ§ЯрЕШЃЌDдзгЕФзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФ3БЖЁЃ
ЃЈ1ЃЉЧыаДГіетЫФжждЊЫидЊЫиУћГЦЃКA_____ЃЛB_____ЃЛC_____ЃЛD_____ЁЃ
ЃЈ2ЃЉAгыCаЮГЩГЃМћЛЏКЯЮяЕФЛЏбЇЪНЪЧ_____ЃЌИУЛЏКЯЮяЕФЫЎШмвКГЪ_____адЁЃ
ЃЈ3ЃЉBгыDаЮГЩЕФЛЏКЯЮяФмШмгкЫЎЃЌЧвгыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЪЧ_____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛиД№ЯТСаЮЪЬтЃКШчЭМЫљЪОЪЧЗжРыЛьКЯЮяЪБГЃгУЕФвЧЦїЃЌЛиД№ЯТСаЮЪЬтЃК
![]()
![]()
![]()
![]()
ЃЈ1ЃЉаДГівЧЦїAЁЂEЕФУћГЦ__ЁЂ__ЁЃ
ЃЈ2ЃЉШєЯђCзАжУжаМгШыЕтЫЎКЭЩйСПCCl4ЃЌеёЕДКѓОВжУЃЌЛсЙлВьЕНЕФЯжЯѓЪЧ__ЁЃ
ЃЈ3ЃЉШєДжбЮШмвКжаКЌгаЩйСПЕФCaCl2ЁЂMgCl2ЁЂMgSO4ЃЌЮЊГ§ЕєетаЉдгжЪЃЌашвРДЮМгШыЕФЛЏбЇЪдМСЪЧNaOHЁЂ__ЁЂ__ЁЂHClЃЈаДЛЏбЇЪНЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЪЕбщВйзїЁЂЯжЯѓгыНсТлЖдгІЙиЯЕе§ШЗЕФЪЧ
бЁЯю | ЪЕбщВйзї | ЪЕбщЯжЯѓ | НсТл |
A | ЯрЭЌЮТЖШЯТЃЌЭЌЪБЯђ Ђй4 mL 0.1 molL-1 KMnO4ЫсадШмвККЭЂк4 mL 0.2 molL-1 KMnO4ЫсадШмвКжаЃЌЗжБ№МгШы4 mL 1 molL-1 H2C2O4ШмвК | ЂйжаШмвКЯШЭЪЩЋ | ИУЪЕбщЬѕМўЯТЃЌKMnO4ХЈЖШдНаЁЃЌЗДгІЫйТЪдНПь |
B | ЯђУКТЏжазЦШШЕФУКЬПЩЯШїЩйСПЫЎ | ВњЩњЕРЖЩЋЛ№бцЃЌУКЬПШМЩеИќЭњ | МгЩйСПЫЎКѓЃЌПЩЪЙУКЬПШМЩеЗХГіИќЖрЕФШШСП |
C | МгШШ2NO2(g) | беЩЋМгЩю | жЄУїе§ЗДгІЪЧЗХШШЗДгІ |
D | ЗжБ№ВтЖЈЪвЮТЯТЕШЮяжЪЕФСПХЈЖШЕФNa2SO3гыNa2CO3ШмвКЕФpH | КѓепНЯДѓ | жЄУїЗЧН№Ъєад SЃОC |
A.AB.BC.CD.D
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com