
【题目】常温下,向1LpH=10的NaOH溶液中持续通入CO2。通入的CO2的体积(V)与溶液中水电离出的OH-离子浓度(φ)的关系如图所示。下列叙述正确的是
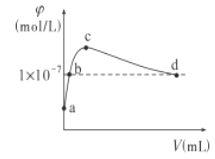
A.a点溶液中:水电离出的c(H+)=1×10-10mol/L
B.b点溶液中:n(Na+)=1×10-10mol
C.c点溶液中:c(Na+)>c(![]() )>c(
)>c(![]() )
)
D.d点溶液中:c(Na+)=2c(![]() )+c(
)+c(![]() )
)
【答案】AD
【解析】
A.a点溶液为1LpH=10的NaOH溶液,溶液中氢离子浓度为1×10-10mol·L-1,就是水电离出的,故A正确;
B.b点溶液中的钠离子全部来自于1LpH=10的NaOH溶液,故![]() ,故B错误;
,故B错误;
C.c点溶液中水电离出的氢氧根离子浓度最大,说明溶液为碳酸钠,根据碳酸根要水解,离子在溶质中出现在前,不出现在后分析,溶液中离子浓度关系为:c(Na+)>c(CO32-)>c(HCO3-),故C错误;
D.d点溶液为碳酸氢钠和碳酸的混合液,此时溶液呈中性,电荷守恒为c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),c(OH-)= c(H+)=1×10-7mol·L-1,则:c(Na+)=2c(CO32-)+c(HCO3-),故D正确。
故选AD。


科目:高中化学 来源: 题型:
【题目】在周期表中,锗和硅位于同主族。四氯化锗(GeCl4)是光导纤维的掺杂剂,其熔点为-49.5℃, 沸点为83.1℃;易水解,对上呼吸道及皮肤有刺激作用。实验室制备四氯化锗的原理是:Ge+2Cl2=GeCl4。某课题组同学拟选择下列装置设计实验制备四氯化锗(部分加热装置和夹持装置省略)。回答下列问题:
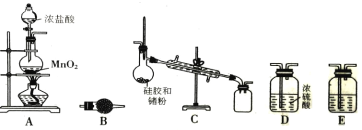
(1)写出A装置中发生反应的化学方程式_______________。
(2)若气体从左到右流动,则装置连接顺序为A、_______________。
(3)C装置中用于冷凝四氯化锗蒸气的仪器名称是_______________,B装置中的试剂是_______________。
(4)E装置中的试剂是_______________,其作用是_______________。
(5)下列有关说法正确的是_______________。
①实验中,先通入氯气,后加热C中烧瓶
②C装置中温度计的温度控制在49℃左右
③观察到D瓶有气泡和液面上有黄绿色气体
④C装置中硅胶的主要作用可能是干燥产品
(6)四氯化锗遇水蒸气产生一种强酸和一种弱酸。实验室用足量NaOH溶液吸收尾气中少量四氯化锗气体,写出该反应的化学方程式:__________________。
(7)实验中消耗m g 纯锗粉制得a g GeCl4,则锗的利用率为_______________(用含 m、a 的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像能说明或反映其对应关系的是( )
|
|
|
|
A | B | C | D |
A.第二周期元素的化合价变化
B.第ⅦA族元素简单阴离子的半径变化
C.向50 mL 0.5mol·L-1NaOH溶液中逐滴加入等浓度盐酸时溶液的pH变化
D.Al与稀硫酸反应产生H2的体积变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CPAE是蜂胶的主要活性成分,由咖啡酸合成CPAE路线如下:
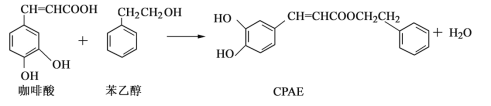
下列说法正确的是
A.可用金属Na检测上述反应是否残留苯乙醇
B.与苯乙醇互为同分异构体的酚类物质共有9种
C.1 mol咖啡酸最多可与含3 mol NaHCO3的溶液发生反应
D.咖啡酸、苯乙醇及CPAE都能发生取代、加成和氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关同分异构体的说法正确的是
A.甲醇在铜催化和加热条件下生成的产物不存在同分异构体
B.2-氯丁烷(CH3CHClCH2CH3)与NaOH乙醇溶液共热,得到三种烯烃。
C.有机物![]() 的同分异构体中,其中属于酯且苯环上有2个取代基的同分异构体有2种。
的同分异构体中,其中属于酯且苯环上有2个取代基的同分异构体有2种。
D.分子式为C5H10O2的有机物中含有![]() 结构的同分异构体有12种
结构的同分异构体有12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】兴趣小组在实验室中模拟利用甲烷和氯气发生取代反应制取副产品盐酸,设计如图装置,下列说法错误的是( )
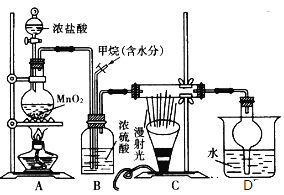
A.实验时先点燃A处酒精灯再通甲烷
B.装置B有均匀混合气体、控制气流速度、干燥混合气体等作用
C.从D中分离出盐酸的方法为过滤
D.装置C经过一段时间的强光照射后,生成的有机物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇燃料电池是目前应用比较广泛的一种燃料电池,其工作原理如下图所示:

下列说法正确的是( )
A.N为正极,发生氧化反应
B.a为氧气,b为甲醇
C.甲池溶液pH增大,乙池溶液pH减小
D.若有1 mol CO2生成,则有6 mol H+从甲池透过交换膜进入乙池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锰在电解锰、染料、造纸以及陶瓷等工业生产中有广泛的应用。利用软锰矿(主要成分为MnO2,含铁的化合物等杂质)和闪锌矿(主要成分ZnS)制得硫酸锰的流程如下:
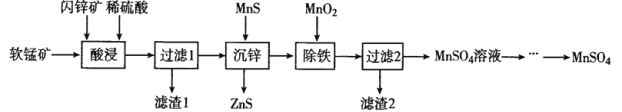
已知:常温下,Ksp(ZnS)=1.2×l0-24、Ksp(MnS)=1.5×10-15
关于该流程说法错误的是
A.“酸浸”时,为了缩短浸取时间,常加入少量FeSO4溶液,FeSO4的作用可能是作催化剂。
B.“沉锌”反应为:Zn2+(aq)+MnS(s)![]() ZnS(s)+Mn2+(aq),该反应的平衡常数K为1.25×109
ZnS(s)+Mn2+(aq),该反应的平衡常数K为1.25×109
C.“除铁”时加二氧化锰是为了氧化Fe2+,然后向溶液加适量氨水将溶液pH调节为3~4
D.该流程中可以循环利用的物质是ZnS
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国家有色金属工业“十三五”发展规划要求,再生铅占铅总量比重到2020年升至45%。从废旧铅蓄电池中回收的工艺流程为![]() ,电解原理如图所示。下列说法错误的是
,电解原理如图所示。下列说法错误的是
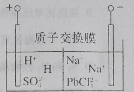
A.电解过程中阳极附近pH明显增大
B.阴极电极反应式为![]() +2e-=Pb+4Cl-
+2e-=Pb+4Cl-
C.电路中通过2 mol电子,阴极可得207 g铅
D.Na2PbCl4浓度下降后,在阴极区加入PbO,可实现电解质溶液的再生使用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com