
【题目】地壳中含量第一和第三的两元素形成的化合物不具有的性质是( )
A.熔点很高B.与铁在高温下发生放热反应
C.能溶于氢氧化钠溶液D.熔融后可以导电
科目:高中化学 来源: 题型:
【题目】某无色溶液中只可能含有K+、Ag+、Ba2+、Cu2+、Cl-、OH-、CO ![]() 、SO
、SO ![]() 中的一种或几种,对其进行如下实验操作:( )
中的一种或几种,对其进行如下实验操作:( )
⑴取少量溶液,滴加无色酚酞试液,酚酞变红;
⑵另取少量溶液,加入足量BaCl2溶液,产生白色沉淀;
⑶向(2)所得混合物中加足量盐酸,沉淀部分溶解,并有无色气体生成;
⑷将(3)所得混合物过滤,向滤液中加入AgNO3溶液,有白色沉淀生成。
下列对该溶液的说法正确的是
A.一定含有OH-、CO ![]() 、SO
、SO ![]() 、Cl-
、Cl-
B.可能含有K+、Cl-
C.一定不含有Ag+、Ba2+、Cu2+
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:
CO(g)+H2O(g) ![]() CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= , 该反应为反应(选填“吸热”、“放热”).
(2)能判断该反应是否达到化学平衡状态的依据是;
A.容器中压强不变
B.混合气体中c(CO)不变
C.v逆(H2)=v正(H2O)
D.c(CO2)=c(CO)
(3)830℃时,容器中的反应已达到平衡.在其他条件不变的情况下,在此温度下,若该容器中含有1molCO2、1.2molH2、0.75molCO、1.5molH2O,这状态(是或否)处于平衡状态?若不是,反应向哪个方向进行? . (选填“向正反应方向”、“向逆反应方向”).
(4)若830℃时,向容器中充入lmolCO、5molH2O,反应达到平衡后,CO的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水AlCl3是一种重要的化工原料.某课外探究小组尝试制取无水AlCl3 , 查阅资料获得下列信息:无水AlCl3在178℃升华,极易潮解,遇水蒸气产生白色烟雾.
探究一 无水AlCl3的实验室制备
利用如图装置,用干燥、纯净的氯气在加热条件下与铝粉(已除去氧化膜)反应制取无水AlCl3 . 供选择的药品:①铝粉 ②浓硫酸 ③稀盐酸 ④饱和食盐水 ⑤二氧化锰粉末 ⑥无水氯化钙 ⑦稀硫酸 ⑧浓盐酸 ⑨氢氧化钠溶液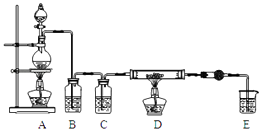
(1)写出装置A烧瓶中发生的反应方程式 .
(2)实验开始前,先检查装置气密性,后装入药品,接下来的步骤依次是(填序号)
a.加热D中硬质玻璃管 b.往A烧瓶中加入液体 c.点燃A中的酒精灯
(3)写出无水AlCl3与水蒸气反应的化学方程式 .
探究二 无水AlCl3的含量测定及结果分析
取D中反应后所得固体2.0g,与足量氢氧化钠溶液反应,测定生成气体的体积(体积均换算成标准状况),重复测定三次,数据如表:
第一次实验 | 第二次实验 | 第三次实验 | |
D中固体用量 | 2.0g | 2.0g | 2.0g |
氢气的体积 | 334.5mL | 336.0mL | 337.5mL |
(4)根据表中数据,计算所得固体中无水AlCl3的质量分数 .
(5)有同学认为测得的无水AlCl3的质量分数偏低,你认为可能的原因有:(填序号)
①制备的氯气不足,②固体和气体无法充分接触,③无水AlCl3发生升华,造成损失.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数,下列叙述中正确的是( )
A.在标准状况下,1L庚烷完全燃烧后,所生成的气态产物的分子数为 ![]() NA
NA
B.1mol碳正离子CH5+所含的电子数为10NA
C.56g铁粉在1mol氯气中充分燃烧,失去的电子数为3NA
D.0.5molC3H8分子中含C﹣H共价键2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W有如下所示的转化关系,且△H=△H1+△H2 , 则X、Y可能是( )
①C,CO ②S,SO2 ③AlCl3、Al(OH)3 ④Na2CO3、NaHCO3 ⑤Fe、FeCl2 . ![]()
A.①②③④⑤
B.②④⑤
C.①③④
D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置的说法中正确的是( )
A.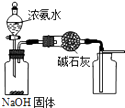
用图装置制取干燥纯净的NH3
B.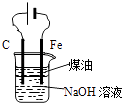
用图装置实验室制备Fe(OH)2
C.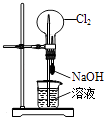
用图装置可以完成“喷泉”实验
D.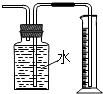
用图装置测量Cu与浓硝酸反应产生气体的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海带中提取碘,有甲、乙两种实验方案如图1:已知:3I2+6NaOH=5NaI+NaIO3+3H2O.请回答: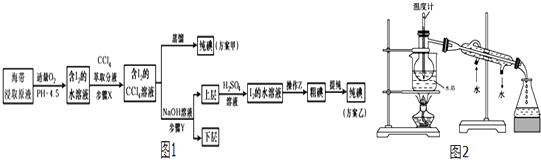
(1)步骤X使用分液漏斗前须检漏,检漏方法为 .
(2)用图所示装置进行蒸馏.指出如图所示实验装置 中的任意两处错误:① .
(3)进行上述操作时,使用水浴加热更好的原因是;最后碘晶体在里聚集.
(4)下列有关步骤Y的说法,正确的是 .
A.应控制 NaOH 溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH 溶液可以由乙醇代替
(5)方案乙在上层溶液中加入H2SO4溶液得到I2的水溶液发生的反应方程式是:;
(6)操作Z的名称是 .
(7)工业中采用方案乙从海带中提取碘,方案甲中采用蒸馏不合理,理由是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com