
| W | X | Y | Z | |
| �ṹ�� ���� | ����������Ӧ��ˮ����������̬�⻯�ﷴӦ�õ����ӻ����� | ��ɫ��Ӧ �ʻ�ɫ | ��ͬ��������Ԫ���γɵļ������У����Ӱ뾶��С���������������Ϊ���������� | ��������������֮��Ϊ�� |
 ������Ӧ��ˮ������Y����������ﷴӦ�����ӷ���ʽΪAl2O3+2OH-=2AlO2-+H2O��
������Ӧ��ˮ������Y����������ﷴӦ�����ӷ���ʽΪAl2O3+2OH-=2AlO2-+H2O��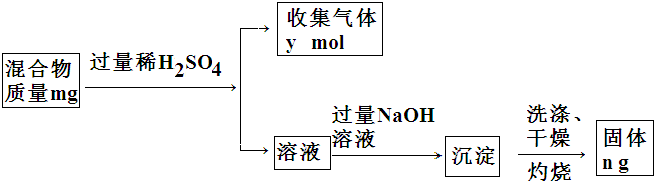
���� W����������Ӧ��ˮ����������̬�⻯�ﷴӦ�õ����ӻ������W��NԪ�أ�X��ɫ��Ӧ�ʻ�ɫ����X��NaԪ�أ�Y��ͬ��������Ԫ���γɵļ������У����Ӱ뾶��С���������������Ϊ�������������Y��AlԪ�أ�Z��������������֮��Ϊ�㣬��Z��ԭ����������Y�Ķ�����Ԫ�أ���Z��SiԪ�أ�������ʽṹ�����ʽ�ɣ�
��� �⣺W����������Ӧ��ˮ����������̬�⻯�ﷴӦ�õ����ӻ������W��NԪ�أ�X��ɫ��Ӧ�ʻ�ɫ����X��NaԪ�أ�Y��ͬ��������Ԫ���γɵļ������У����Ӱ뾶��С���������������Ϊ�������������Y��AlԪ�أ�Z��������������֮��Ϊ�㣬��Z��ԭ����������Y�Ķ�����Ԫ�أ���Z��SiԪ�أ�
��1��Z��SiԪ�أ����������4�����ӣ�����������Ԫ�أ����Դ��ڵ������ڵ�IVA�壬�ʴ�Ϊ���������ڵڢ�A�壻
��2��Na�����������Ϊ�����ƣ�Na2O�������Ӻ�������֮��ͨ�����Ӽ��γɵ����ӻ��������ʽΪ ��Al�����������Ϊ��������������Ϊ������������������Ʒ�Ӧ����ƫ�����ƣ����ӷ�Ӧ����ʽΪAl2O3+2OH-=2AlO2-+H2O��
��Al�����������Ϊ��������������Ϊ������������������Ʒ�Ӧ����ƫ�����ƣ����ӷ�Ӧ����ʽΪAl2O3+2OH-=2AlO2-+H2O��
�ʴ�Ϊ�� ��Al2O3+2OH-=2AlO2-+H2O��
��Al2O3+2OH-=2AlO2-+H2O��
��3���������ڹ��ۻ����Ԫ�صķǽ�����Խǿ���Ӧ�⻯���ȶ���Խǿ�����ڷǽ�����N��Si������̬�⻯����ȶ���ΪNH3��SiH4��HN3�������������൱����HN3Ϊ���ᣬ��NaOH�����кͷ�Ӧ������ʽΪHN3+NaOH=NaN3+H2O��
�ʴ�Ϊ�����ۣ�NH3��SiH4��HN3+NaOH=NaN3+H2O��
��4��þ������ϡ���ᷴӦ��������þ��������������������þ��������������������Һ��Ӧ����������þ�����������������������������Ʒ�Ӧ����ƫ�����ƣ�������þ������������Һ����Ӧ������������þ���壬������þ�ֽ���������þ��ˮ������������ù���������þ��
a������n��������þ������������m��n�������������Ӷ�����������������������ȷ��
b������þ������������þ����ϡ���ᷴӦ��������������������þ�������Ӷ�����������������������ȷ��
c������n����������þ������������þ��������þ��ϡ���ᷴӦ���������������Ӷ��ó�����ϡ���ᷴӦ���������������ʶ��ó�������������������ȷ��
��ѡabc��
���� ���⿼��ṹ����λ�ù�ϵ������ʽ��д����Ԫ�ػ���������ԡ�����ˮ�⡢Ԫ�ػ��������ʵȣ��Ѷ��еȣ��ƶ�Ԫ���ǽ���ؼ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� NaHCO3 ��Һ��һ�μ����ϡ���ᡢNaOH��Һ��AlCl3��Һ��NaAlO2 ��Һ | |
| B�� | ��������Լ�ƿ�ڱ��Ϻ�ɫ���ʿ���ϡ����ϴ�� | |
| C�� | ��ȥSO2 ������HCl������ͨ�뱥�͵�Na2SO3 ��Һ | |
| D�� | ������茶�������ˮ�����ˮ���½���֤�������ˮ�������ȵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C2H2 | B�� | C2H6O | C�� | C4H6 | D�� | C2H4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
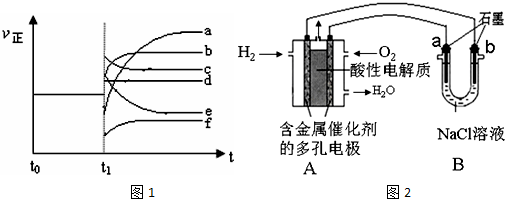
| ������� | c��H2O��/mol•L-1 | c��CO��/mol•L-1 | c��H2��/mol•L-1 | �����������Ƚ� |
| I | 0.06 | 0.60 | 0.10 | ����=���� |
| �� | 0.12 | 0.20 | ��0.6 | ����=���� |
| �� | 0.10 | 0.20 | 0.40 | �ڦ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | A | B | CO | H2 |
| ȼ����/kJ•mol-1 | 725 | 5 518 | 283 | 286 |
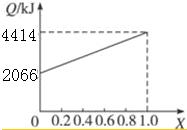
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C4H10 | B�� | CH2Cl2 | C�� | C2H4O2 | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���û������������Ӽ��γɣ�
���û������������Ӽ��γɣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ϸ�Ӧ���ɷ��� | B�� | ֻ�Т߲��ܷ��� | ||
| C�� | ֻ�Т��ܷ��� | D�� | ֻ�Тڲ��ܷ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com