
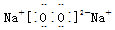 ;AB2的结构式是O=C=O.
;AB2的结构式是O=C=O.分析 A、B、C、D、E、F的原子序数逐渐增大,A原子最外层电子数是内层电子数的二倍,则A为碳元素,A和F同族,则F为硅元素,A和B同周期,B元素族序数是周期数的三倍,则B为氧元素,B的阴离子与C、D、E的简单阳离子电子层结构相同,则C为钠元素,D是镁元素、E是铝,据此答题.
解答 解:(1)硅在元素周期表中的位置是第三周期第ⅣA族,故答案为:第三周期第ⅣA族;
(2)过氧化钠的电子式是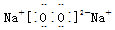 ;二氧化碳的结构式是O=C=O,故答案为:
;二氧化碳的结构式是O=C=O,故答案为: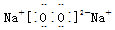 ; O=C=O;
; O=C=O;
(3)电子层数越多,离子半径越大,电子层数相同时,核电荷数越多,离子半径越小,所以B、C、D、E离子半径的由大到小的顺序为O2->Na+>Mg2+>Al3+,元素的金属性越强,对应的最高价氧化物对应水化物的碱性就越强,金属性Na>Mg>Al,所以碱性NaOH>Mg(OH)2>Al(OH)3,
故答案为:O2->Na+>Mg2+>Al3+; NaOH>Mg(OH)2>Al(OH)3;
(4)钠、铝最高价氧化物对应水化物能够相互反应,即氢氧化钠和氢氧化铝反应,其离子方程式为Al(OH)3+OH-=AlO2-+2 H2O,
故答案为:Al(OH)3+OH-=AlO2-+2 H2O.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,侧重对基础知识的巩固,注意对基础知识的掌握.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:多选题
| A. | 酸性氧化物:CO2、SO2、H2O | B. | 碱性氧化物:Na2O、CaO、P2O5 | ||
| C. | 碱:NaOH、KOH、Ba(OH)2 | D. | 铵盐:NH4Cl、NH4NO3、(NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
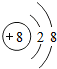 .写出元素Z的气态氢化物的电子式
.写出元素Z的气态氢化物的电子式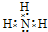 (用元素符号表示)
(用元素符号表示)查看答案和解析>>
科目:高中化学 来源: 题型:实验题
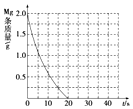 为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20mol•L-1与0.40mol•L-1的HCl溶液、0.20mol•L-1与0,.40mol•L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20mol•L-1与0.40mol•L-1的HCl溶液、0.20mol•L-1与0,.40mol•L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.| 实验 编号 | 温度(K) | 盐酸浓度/ (mol•L-1) | 醋酸浓度/ (mol•L-1) | 实验目的 |
| a | 298 | 0.20 | I.实验a和b是探究温度 对镁与盐酸反应速率的影响; II.实验a和c是探究浓度 对镁与盐酸反应速率的影响; III.实验a和d是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别 | |
| b | 308 | 0.20 | ||
| c | 298 | 0.40 | ||
| d | -- | -- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
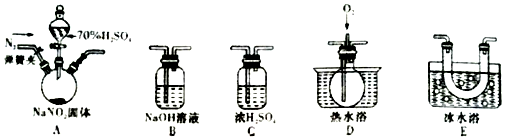
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
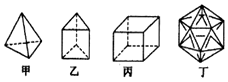
| A. | 1mol甲分子内含有10mol共价键 | B. | 乙分子的一氯取代产物只有一种 | ||
| C. | 丙分子的二氯取代产物只有两种 | D. | 丁分子显然是不可能合成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应是置换反应 | B. | 该反应是复分解反应 | ||
| C. | CO发生氧化反应 | D. | NO是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3+H2O+CO2=NH4HCO3 | |
| B. | 2NH3+CO2$\frac{\underline{\;180-200℃\;}}{15-30MPa}$ CO(NH2)2+H2O | |
| C. | 8NH3+3Cl2═N2+6NH4Cl | |
| D. | 2NH3+2O2$\frac{\underline{\;一定条件\;}}{\;}$NH4NO3+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com