
| 选项 | 实验器材(省略夹持装置) | 相应实验 |
| A | 三脚架、泥三角、坩埚、坩埚钳 | 煅烧石灰石制取生石灰 |
| B | 烧杯、玻璃棒、胶头滴管、100mL容量瓶 | 用浓盐酸配制100mL 0.1mol?L-1的稀盐酸溶液 |
| C | 烧杯、玻璃棒、分液漏斗 | 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸和乙醇 |
| D | 烧杯、酸式滴定管、碱式滴定管 | 用H2SO4标准液滴定未知浓度的NaOH溶液 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
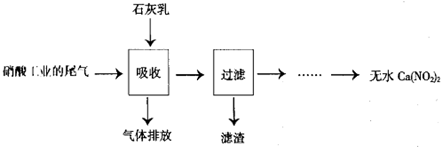
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+、Na+、Br- |
| B、NH4+、Na+、AlO2- |
| C、Ba2+、Al3+、Cl- |
| D、K+、Mn4-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酒精在实验台上燃烧时,用水扑灭火焰 |
| B、给试管中的液体加热时,试管口不能对着别人 |
| C、大量有毒易燃气体在室内扩散,应立即打开排气扇开关 |
| D、不慎将浓硫酸沾到皮肤上,应用较多的水冲洗,然后涂上硼酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛 | ||
| B、不慎将浓碱液沾到皮肤上,要立即用大量水冲洗,然后涂上小苏打溶液 | ||
C、在加热的情况下,试管中的液体体积不要超过试管容积的
| ||
| D、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、福尔马林可作食品的保鲜剂 |
| B、氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应 |
| C、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| D、浓硫酸可刻蚀石英制艺术品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢铁生锈与氧气、水蒸气有关,且以吸氧腐蚀为主 |
| B、氢氧化钠固体潮解、变质与水蒸气、二氧化碳有关 |
| C、浓硫酸露置于空气中浓度变小,与水蒸气有关 |
| D、钢铁在潮湿的空气中发生电化腐蚀,其正极的电极反应式为Fe-2e=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
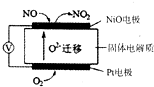 NO2是汽车尾气中的主要污染物之一.
NO2是汽车尾气中的主要污染物之一.
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com