
| A. | 32g O2所含的原子数目为NA | |
| B. | 0.5mol H2O含有的原子数目为1.5NA | |
| C. | 常温常压下,4.4g CO2 与N2O混合气体中含有的原子总数为0.3NA | |
| D. | 0.5NA个氯气分子的物质的量是0.5mol |
分析 A、氧气由氧原子构成;
B、水为三原子分子;
C、CO2 与N2O的摩尔质量均为44g/mol,且均为三原子分子;
D、物质的量n=$\frac{N}{{N}_{A}}$.
解答 解:A、氧气由氧原子构成,故32g氧气中含有的氧原子的物质的量为2mol,故为2NA个,故A错误;
B、水为三原子分子,故0.5mol水中含1.5NA个原子,故B正确;
C、CO2 与N2O的摩尔质量均为44g/mol,故4.4g混合物的物质的量为0.1mol,且两者均为三原子分子,故0.1mol混合物中含0.3NA个原子,故C正确;
D、物质的量n=$\frac{N}{{N}_{A}}$=$\frac{0.5{N}_{A}}{{N}_{A}/mol}$=0.5mol,故D正确.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 将53gNa2CO3溶于水配成500mL溶液 | |
| B. | 将40g氢氧化钠溶于1L水中 | |
| C. | 将1L10mol/L的NaCl溶液溶于9L水中 | |
| D. | 将22.4LHCl溶于水配成1L溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体摩尔体积就是22.4 L•mol-1 | |
| B. | 1 mol H2所占的体积约为22.4 L | |
| C. | 在标准状况下,1 mol H2O(g)的体积是22.4 L | |
| D. | 在标准状况下,1 mol NH3和CO混合气体所占的体积约为22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
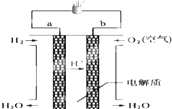 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 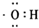 为羟基的电子式,也是氢氧根离子的电子式 为羟基的电子式,也是氢氧根离子的电子式 | |
| B. | S2-的结构示意图: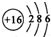 | |
| C. | 甲烷分子的比例模型是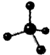 | |
| D. | 中子数为10的氧原子:18O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只要有一种反应物的键能大于一种生成物的键能,这个反应就是放热反应 | |
| B. | 只要有一种反应物的键能大于一种生成物的键能,这个反应就是吸热反应 | |
| C. | 反应物的键能之和比生成物的键能之和大得越多,反应放出的能量就越多 | |
| D. | 反应物的键能之和比生成物的键能之和大得越多,反应吸收的能量就越多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①②④ | C. | ①② | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+2O2→CO2+2H2O+311.4kJ | B. | CH4(g)+2O2(g)→CO2(g)+2H2O(l)+311.4kJ | ||
| C. | CH4(g)+2O2(g)→CO2(g)+2H2O(l)+889.7kJ | D. | CH4(g)+2O2(g)→CO2(g)+2H2O(g)+889.7kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com