
| A�� | һ��û��Na2CO3��Ba��NO3��2 | |
| B�� | һ����Na2CO3��û��Ba��NO3��2 | |
| C�� | û��Ba��NO3��2����KNO3�����ܻ���Na2CO3 | |
| D�� | û��Na2CO3����Ba��NO3��2��KNO3 |
���� �������֪��ȡ��Ʒ����ˮ�еõ�������Һ�����������ᱵ������������Ȼ�����Һ�ܲ���������Ȼ����ݳ�����������һ��ȷ��̼���ƺ�����صĴ��ڣ�
��� �⣺��Ʒ����ˮ�еõ�������Һ��˵��һ�������ᱵ��
����7.8g��̼��ز���̼��Ƶ�����Ϊx������
K2CO3+CaCl2�TCaCO3��+2KCl
138 100
7.8g x
$\frac{138}{7.8g}=\frac{100}{x}$ x=5.65g
����7.8g��̼���Ʋ���̼��Ƶ�����Ϊy������
Na2CO3+CaCl2�TCaCO3��+2NaCl
106 100
7.8g y
$\frac{106}{7.8g}=\frac{100}{y}$ y��7.36g
������̼������õ�����������Ӧ�ô���5.65gС��7.36g����ʵ��ֻ�õ�5.0g���ʲ����ܺ���̼���ƣ�һ����������أ�
��ѡA��
���� ���⿼���˸��ݸ��ֽⷴӦ�ж����ʹ�������⣬�Լ����ݻ�ѧ����ʽ�ļ��㣬���жϻ��������ʱ���ɲ��ü�ֵ����ƽ��ֵ����


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
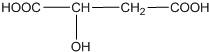 ���������кȹ��ף�ƻ������һ����ƻ�����Ͷ��ɵľ��нⶾ����֬�����ʺ�ֹк������ҩЧ�Ľ���ʳƷ��ƻ�������������ϵ���Ҫ�������ʣ�ƻ����Ľṹ��ͼ��ʾ���������˵������ȷ���ǣ�������
���������кȹ��ף�ƻ������һ����ƻ�����Ͷ��ɵľ��нⶾ����֬�����ʺ�ֹк������ҩЧ�Ľ���ʳƷ��ƻ�������������ϵ���Ҫ�������ʣ�ƻ����Ľṹ��ͼ��ʾ���������˵������ȷ���ǣ�������| A�� | ƻ������һ���������ܷ���������Ӧ | |
| B�� | ƻ������һ���������ܷ�����������Ӧ | |
| C�� | ƻ������һ���������ܷ�����ȥ��Ӧ | |
| D�� | 1molƻ��������������ã�����ܲ���3mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��0.05+a�� mol | B�� | 0.5a mol | C�� | 0.1a mol | D�� | 2a mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
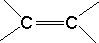 ���еĦм�����������ת�����CH3CH=CHCH3������˳���칹�壮�յ����ŵķ��ӽṹ��ͼ1��ʾ������������ԭ���У���С�������������ͬһƽ���ϣ�������һ˳���칹��Ľṹ��ʽΪ
���еĦм�����������ת�����CH3CH=CHCH3������˳���칹�壮�յ����ŵķ��ӽṹ��ͼ1��ʾ������������ԭ���У���С�������������ͬһƽ���ϣ�������һ˳���칹��Ľṹ��ʽΪ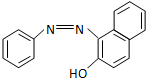 ���յ�������ˮ�е��ܽ�Ⱥ�С�������Ҵ��������ǻ�ȡ���ڶ�λ�γ�ͼ2��ʾ�ṹ�������ܽ�Ȼ������۵����ߣ�����ߡ����͡����������������ʵ��������ʴ������������ԭ��������յ���I���γɷ���������������κ�ķ����γɷ��Ӽ���������Ӽ�������������ӷ��Ӽ����������Ӷ���������������ܽ�Ⱥ�����۵㣮
���յ�������ˮ�е��ܽ�Ⱥ�С�������Ҵ��������ǻ�ȡ���ڶ�λ�γ�ͼ2��ʾ�ṹ�������ܽ�Ȼ������۵����ߣ�����ߡ����͡����������������ʵ��������ʴ������������ԭ��������յ���I���γɷ���������������κ�ķ����γɷ��Ӽ���������Ӽ�������������ӷ��Ӽ����������Ӷ���������������ܽ�Ⱥ�����۵㣮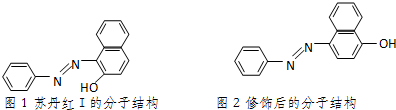
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol H2O������Ϊ18g/mol | B�� | 3.01��1023��SO2���ӵ�����Ϊ32g | ||
| C�� | CH4��Ħ������Ϊ16g | D�� | 44g CO2���е�Oԭ����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ϡ���������۷�Ӧ��Fe+2H+=Fe2++H2�� | |
| B�� | ̼�ᱵ���ڴ��BaCO3+2H+=Ba2++H2O+CO2�� | |
| C�� | пƬ������������Һ�У�Zn+2Ag+=Zn2++2Ag | |
| D�� | ����ͭ��Һ������������Һ��Ӧ��Ba2++SO42-=BaSO4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
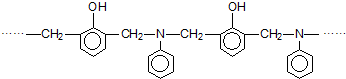
| A�� | 3�ֵ���ͨ���Ӿ۷�Ӧ�ۺ� | B�� | �γɸû�����ĵ���ֻ��2�� | ||
| C�� | ����һ�ֵ���Ϊ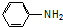 | D�� | ����һ�ֵ���Ϊ1��5-�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
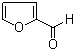 ૼ�ȩ������ȩ���Ľṹ��ʽ��ͼ��������еĻ��ͱ��������ƵĻ�ѧ���ʣ����С������ԡ���������ڿ�ȩ������������ǣ�������
ૼ�ȩ������ȩ���Ľṹ��ʽ��ͼ��������еĻ��ͱ��������ƵĻ�ѧ���ʣ����С������ԡ���������ڿ�ȩ������������ǣ�������| A�� | ������ૼ״� | B�� | ������ૼ��� | ||
| C�� | ������ˮ���ɶ��ּӳɲ��� | D�� | ���뱽���Ʊ���ȩ��֬ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com