
能正确表示下列反应离子方程式的是( )
A.NaNO2 溶液中加入酸性 KMnO4 溶液:2MnO4- + 5NO2- +6H+= 2Mn2+ + 5NO3- + 3H2O
B.碳酸氢铵溶液中加入足量氢氧化钡溶液:NH4+ +HCO3- +2OH- =CO32- +NH3 • H2O+ H2O
C.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I- =2Fe2+ +I2
D.用铜作电极电解饱和氯化钠溶液:2C1- +2H2O=Cl↑+H2↑ +2OH-
科目:高中化学 来源:2015-2016学年河北省唐山市高一下期末化学试卷(解析版) 题型:选择题
恒温下,在体积恒定的密闭容器中发生可逆反应:2SO2 (g)+ O2 (g)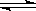 2SO3(g),下列不能用来判断该反应达到平衡状态的是
2SO3(g),下列不能用来判断该反应达到平衡状态的是
A.容器中压强不再变化
B.SO2的体积分数不再变化
C.容器中各物质的浓度不再变化
D.单位时间内生成SO2的物质的量与消耗SO3的物质的量相等
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省宁德市高二下期末化学试卷(解析版) 题型:选择题
据报道美国准备试验绿色航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,结构如图,它比肼燃烧释放能量更高,更安全、环保。下列说法不正确的是( )

A.羟基硝酸铵中各原子共平面
B.固态时羟基硝酸铵是离子晶体
C.羟基硝酸铵中含有离子键和共价键
D.9.6g羟基硝酸铵中含有0.2NA个离子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省周口市高二下期末化学试卷(解析版) 题型:填空题
【化学-选修3:物质结构与性质】
I .已知A、B、C、D、E、F为元素周期表中前四周期且原子序数依次增大的六种元素。其中A、B、C、D核电荷数之和为36, A、C原子的最外层电子数之和等于B原子的次外层电子数,D原子质子数为B原子质子数的两倍,E元素所在主族均为金属,F的价电子数 与C的核电荷数相等。
(1)下列关于上述几种元素的说法正确的是 。
a.B、C、D的原子半径由大到小的顺序为:D>C>B
B.E、F的最外层电子数相等
c.A、B、C、D四种元素中电负性和第一电离能最大的均为B
d.B与C形成的化合物中可能含有非极性键
e.A、C、F位于周期表的s区
(2)B单质有两种同素异形体。其中在水中溶解度较大的是 (填化学式),原因是 。
(3)EA2和A2B熔点较高的是 (填化学式),原因是 。
(4)D与B可以形成两种分子,其中DB2分子中心原子的杂化类型是 。
下列分子或离子中与DB3结构相似的是 。
a.NH3 B.SO32- C. NO3- D. PCl3
(5)已知B、F能形成两种化合物,其晶胞如图所示。则高温时甲易转化为乙的原因为 。

若乙晶体密度为pg/cm3,则乙晶胞的晶胞参数为a = nm。
Ⅱ.金属在化工生产及日常生活中有着广泛的应用,如铁、铬、镓等在现代工业中备受青睐。
(1)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态Cr原子中,未成对电子数有 个, Cr3+的价电子排布式为 。
(2) Zn与Ga的第一电离能从大到小的顺序为 。
(3)镓与第VA族元素可形成多种新型人工半导体材料, 砷化镓(GaAs)就是其中一种,其晶体结构如右图所示(白色球代表原子)。在GaAs晶体中,距离每个Ga原子最近的As原子有 个,距离每个As原子最近的As原子有 个。

(4)与As同主族的短周期元素是N、P,AsH3 空间构型为 ;一定压强下将AsH3和NH3、PH3的混合气体降温时首先液化的是 ,理由是 。
(5)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如下图所示,则氮化铁的化学为 ;设晶胞边长为acm,阿伏加德罗常数为 ,该晶体的密度为 g•cm-3(用含a和NA的式子表示)。
,该晶体的密度为 g•cm-3(用含a和NA的式子表示)。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省周口市高二下期末化学试卷(解析版) 题型:选择题
为测定某有机物的结构,用核磁共振仪处理后得到如图所示的核磁共振氢谱,则该有机物可能是( )
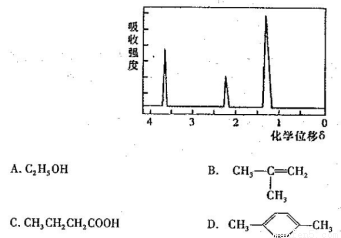
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省周口市高二下期末化学试卷(解析版) 题型:选择题
下列有关实验的做法正确的是 ( )
A. 用pH试纸测氯水的pH
B. 用托盘天平准确称取5.72 g NaCl晶体
C. 用酸式滴定管量取20.00 mL的酸性KMnO,溶液
D. 用带磨口玻璃塞的试剂瓶保存Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省宝鸡市岐山县高一下期末质检化学试卷(解析版) 题型:填空题
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。
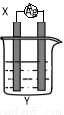
请回答下列问题:
(1) 电极X的材料是______;电解质溶液Y是________;
(2) 银电极为电池的 极,发生的电极反应式为 ;X电极上发生的电极反应为______反应;(填“氧化”或“还原”)
(3) 外电路中的电子 (填“流出”或“流向”)Ag电极。
(4) 当有1.6 g铜溶解时,银棒增重______ g。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省宝鸡市岐山县高一下期末质检化学试卷(解析版) 题型:选择题
我国积极启动“蓝天工程”和“绿水工程”,是为了保护生态环境、提高全体人民生活质量的重要举措。下列措施不利于以上工程实施的是
A.推广使用燃煤脱硫技术,防治SO2污染
B.减少重金属、农药和难分解有机物的排放
C.加大石油、煤炭的开采速度,增加化石燃料的供应量
D.开发新能源和新致冷剂,减少CO2和氟氯烃等物质的大量排放
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省宝鸡市岐山县高二下期末(结构)化学试卷(解析版) 题型:选择题
以下性质的比较中,正确的是( )
A.晶格能大小:NaI > NaBr> NaCl> NaF
B.单质的熔点:Li < Na < K < Rb
C.共价键的键能:C-C > C-Si > Si-Si
D.沸点高低:HF < HCl < HBr < HI
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com