

分析 (1)根据化学平衡状态特征判断分析,达到平衡时,一是等,二是定:
等是指v正=v逆,同一种物质:该物质的生成速率等于它的消耗速率;不同的物质:速率之比等于方程式中各物质的计量数之比,但必须是不同方向的速率;
定是指各成分含量保持不变:各组成成分的质量、物质的量、分子数、体积(气体)、物质的量浓度均保持不变;各组成成分的质量分数、物质的量分数、气体的体积分数均保持不变;若反应前后的物质都是气体,且总体积不等,则气体的总物质的量、总压强(恒温、恒容)、平均摩尔质量、混合气体的密度(恒温、恒压)均保持不变;
(2)相对于曲线b,曲线a的斜率更大,但是最终C2H4的物质的量与曲线b相同,说明a的反应速率更大,只缩短了达平衡的时间,根据影响化学反应速率和化学平衡的条件进行分析;
(3)由图可知:c曲线的斜率更小,达平衡时,C2H4的物质的量减少;所以c曲线的反应速率更慢,其它条件不变,改变温度,速率减慢,则说明改变的条件是降温,再结合降温对平衡的影响进行分析;
(4)0~20min生成C2H4的物质的量为2mol,根据方程式可知生成C2H6的物质的量也是2mol,则C2H6的浓度变化量为$\frac{2mol}{2L}$=1mol•L-1,再根据v(C2H6)=$\frac{△C({C}_{2}{H}_{6})}{△t}$计算反应速率;
(5)燃料电池的负极充入燃料,发生氧化反应,则a为负极;正极充入氧气,发生还原反应,则b为正极;再考虑电解质溶液参加反应写出a电极反应式;c与b相连,与正极相连的是电解池的阳极,阳极发生氧化反应,则铜失去电子生成铜离子,由此写出c极电极反应式.
解答 解:(1)a.达平衡时各物质的量浓度是保持不变,不一定成比例,所以c(C2H6)与c(C2H4)的比值保持不变不一定在平衡,故a错误;
b.由反应C4H10(g)?C2H4(g)+C2H6(g)可知,恒容的容器中气体总物质的量随反应的进行而增大,容器中气体的压强逐渐增大,当容器中气体压强保持不变,说明气体总物质的量保持不变,则达到平衡状态,故b正确;
c.容器的体积一直不变,根据质量守恒,气体的总质量不变,所以气体的密度始终不变,故容器中气体密度保持不变不能说明达到平衡,故c错误;
d.单位时间内有1molC4H10消耗的方向是正方向,同时有1molC2H4生成也是正方向,方向相同,不能说明v正=v逆,不一定达平衡,故d错误;
故答案为:b;
(2)相对于曲线b,曲线a的斜率更大,但是最终C2H4的物质的量与曲线b相同,说明a的反应速率更大,只缩短了达平衡的时间,平衡没有移动,即没有改变化学平衡状态,所以改变的条件应是加入催化剂,
故答案为:加入催化剂,速率加快但平衡没有移动;
(3)由图可知:c曲线的斜率更小,达平衡时,C2H4的物质的量减少;所以c曲线的反应速率更慢,其它条件不变,改变温度,速率减慢,则改变的条件是降温,
由方程式C4H10(g)?C2H4(g)+C2H6(g)可知,降温的同时C2H4的物质的量在减少,说明平衡向逆方向移动,即逆方向是一个放热反应,正方向为吸热反应,
故答案为:吸热;
(4)0~20min生成C2H4的物质的量为2mol,根据方程式可知生成C2H6的物质的量也是2mol,则C2H6的浓度变化量为$\frac{2mol}{2L}$=1mol•L-1,
v(C2H6)=$\frac{△C({C}_{2}{H}_{6})}{△t}$=$\frac{1mol•{L}^{-1}}{20min}$=0.05mol•L-1•min-1,
故答案为:0.05mol•L-1•min-1;
(5)燃料电池的负极充入燃料C2H6,C2H6发生氧化反应,则a为负极;C2H6失去电子生成二氧化碳,二氧化碳与电解质溶液氢氧化钾反应生成碳酸钾,根据电荷守恒写出负极的电极反应式为:C2H6-14e-+18OH-=2CO32-+12H2O;正极充入氧气,发生还原反应,则b为正极;c与b相连,与正极相连的是电解池的阳极,阳极发生氧化反应,则铜失去电子生成铜离子,由此写出c极电极反应式:Cu-2e-=Cu2+,
故答案为:C2H6-14e-+18OH-=2CO32-+12H2O;Cu-2e-=Cu2+.
点评 本题考查化学平衡状态标志的判断,以及影响化学反应速率、化学平衡移动的条件,注意对图象题的理解,还考查化学反应速率的计算,比较简单,原电池与电解池的结合考查,难度适中.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 能使石蕊溶液呈红色的溶液中:Na+、SO42-、Fe3+、MnO4-可以大量共存 | |
| B. | NA代表阿伏加德罗常数的数值,1 mol硫酸氢钾晶体中阳离子所带电荷总数为NA | |
| C. | 235U与238U的相互转化不是化学变化 | |
| D. | 元素O、S、P的气态氢化物热稳定性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
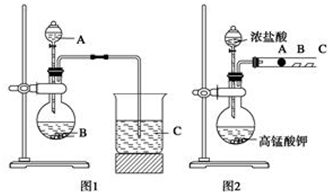
 乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.该组同学的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x值.通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO${\;}_{4}^{-}$+5H2C2O4+6H+═=2Mn2++10CO2↑+8H2O学习小组的同学设计了滴定的方法测定x值.
乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.该组同学的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x值.通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO${\;}_{4}^{-}$+5H2C2O4+6H+═=2Mn2++10CO2↑+8H2O学习小组的同学设计了滴定的方法测定x值.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.02 mol•L-1醋酸与0.02 mol•L-1NaOH等体积混合后的溶液中加少量的CH3COONa固体则$\frac{c(C{H}_{3}CO{O}^{-})}{c(N{a}^{+})}$增大 | |
| B. | 常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H>0 | |
| C. | lmol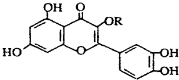 与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4 mol、8 mol 与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4 mol、8 mol | |
| D. | 红外光谱分析不能区分乙醇和乙醚 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 由A和B两种元素形成的化合物BA5中含共价键 | |
| B. | 含C或E元素的某些物质具有杀菌消毒的作用,其原理相同 | |
| C. | 原子半径:D>C>B,离子半径B>C>D | |
| D. | 由A、C、E三种元素形成的某种化合物AEC,其结构式A-E-C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 为证明反应的发生,可取甲中溶液加入酸性高锰酸钾溶液 | |
| B. | 反应开始时,乙中电极反应为2I--2e-=I2 | |
| C. | 电流计读数为零时,反应达到化学平衡状态 | |
| D. | 反应开始时,甲中石墨电极上Fe3+被还原 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com