
下列说法正确的是( )
A.ΔH<0、ΔS>0的反应在任何温度都能自发进行
B.NH4HCO3(s)===NH3(g)+H2O(g)+CO2(g)
ΔH=+185.57 kJ/mol能自发进行,原因是体系有自发地向混乱度增加方向转变的倾向
C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向
科目:高中化学 来源: 题型:
在容积不变的密闭容器中存在如下反应:2A(g)+B(g)  3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )

A.图Ⅰ表示的是t1时刻增大反应物的浓度对反应速率的影响
B.图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高
D.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对聚氯乙烯树脂的用途叙述中,不正确的是( )
A.该树脂加入一定的添加剂后,可以用来制造农用薄膜
B.该树脂加入一定的添加剂后,可以用来制造管材
C.该树脂加入一定的添加剂后,可以用来制造有机玻璃
D.该树脂加入一定的添加剂后,可以用来制造化学纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s) ΔH=-444.3 kJ/mol,且熵减小,在常温常压下该反应能自发进行,对反应的方向起决定作用的是
( )
A.焓变 B.温度
C.压强 D.熵变
查看答案和解析>>
科目:高中化学 来源: 题型:
H2和CO2在高温下发生反应:
CO2(g)+H 2(g)
2(g)  CO(g)+H2O(g)。下表是986℃时,在容积不变的密闭容器中进行反应的四组数据:
CO(g)+H2O(g)。下表是986℃时,在容积不变的密闭容器中进行反应的四组数据:
| 编号 | 起始浓度/mol/L | 平衡浓度/mol/L | ||||||
| c0(H2) | c0(CO2) | c0(H2O) | c0(CO) | c(H2) | c(CO2) | c(H2O) | c(CO) | |
| 1 | 1.0 | 1.0 | 0 | 0 | 0.44 | 0.44 | 0.56 | 0.56 |
| 2 | 1.0 | 2.0 | 0 | 0 | 0.27 | 1.27 | 0.73 | 0.73 |
| 3 | 0 | 0 | 2.0 | 2.0 | 0.88 | 0.88 | 1.12 | 1.12 |
| 4 | 0.2 | 0.4 | 0.6 | 0.8 | 0.344 | 0.544 | 0.456 | 0.656 |
下列叙述中正确的是( )
①该温度下反应的平衡常数约为1.62
②该反应的平衡常数与反应的起始浓度无关
③增大CO2的起始浓度,可使CO2的转化率增大
④从反应开始至达到平衡状态,混合气体的密度没有发生改变
A.②③ B.①②③
C.①②④  D.①③
D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质分类或归类正确的一组是: ( )
①液氨、液氯、干冰、碘化银均为化合物
②氢氟酸、盐酸、水玻璃、氨水均为混合物
③明矾、小苏打、醋酸、次氯酸均为电解质
④碘酒、牛奶、豆浆、漂粉精均为胶体
⑤Na2O2、Na2CO3、NaHCO3、Na2SiO3均为钠盐
⑥CH3COONa 、 Na2CO3 、NaHSO3、NaF溶液均为碱性
A.①和② B.②和③ C.③和④ D.②③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的离子不含电子;B元素的最高价氧化物对应水化物与其氢化物能反应生成盐F;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的3/4,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。请回答下列问题:
(1)E元素在元素周期表中的位置是 。
(2)由A、B、C三种元素形成的离子化合物的化学式为 。
(3)A、C、E间可形成甲、乙两种三原子分子,且甲有18个电子、乙有10个电子,甲与乙比较,沸点较高的是(填化学式) 。
(4)F含有的化学键类型是 和 ,其水溶液呈酸性,请用相关的离子方程式解释其原因 。
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该过程的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
对某酸性溶液(可能含有Br-、SO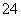 、H2SO3、NH
、H2SO3、NH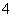 )分别进行如下实验:①加热时放出的气体可以使品红溶液褪色;②加碱调至碱性后,加热时放出的气体可以使湿润的红色石蕊试纸变蓝;③加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸。对于下列物质不能确认其在溶液中是否存在的是 ( )
)分别进行如下实验:①加热时放出的气体可以使品红溶液褪色;②加碱调至碱性后,加热时放出的气体可以使湿润的红色石蕊试纸变蓝;③加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸。对于下列物质不能确认其在溶液中是否存在的是 ( )
A.Br- B.SO42— C.H2SO3 D.NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分子或离子在指定的分散系中能大量共存的一组是
A.银氨溶液:Na+、K+、NO 、NH3·H2O
、NH3·H2O
B.空气:C2H2、CO2、SO2、NO
C.氢氧化铁胶体:H+、K+、S2-、Br-
D.高锰酸钾溶液:H+、Na+、SO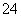 、葡萄糖分子
、葡萄糖分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com