
【题目】已知ClCH=CHCl 有两种结构:![]() 和
和![]() ,像这种由于双键不能自由旋转形成的异构体,叫顺反异构体,下列烯烃存在顺反异构现象的是
,像这种由于双键不能自由旋转形成的异构体,叫顺反异构体,下列烯烃存在顺反异构现象的是
A.CH2=CH2B.CH3CH=CH2
C.CH3CH=CHCH3D.CH3CH=C(CH3)2
科目:高中化学 来源: 题型:
【题目】关于下列几种离子晶体,说法不正确的是( )
A.由于![]() 晶体和
晶体和![]() 晶体中正、负离子半径比
晶体中正、负离子半径比![]() 不相等,所以两晶体中离子的配位数不相等
不相等,所以两晶体中离子的配位数不相等
B.![]() 晶体中,
晶体中,![]() 配位数为8,
配位数为8, ![]() 配位数为4,不相等,主要是由于
配位数为4,不相等,主要是由于![]() 、
、![]() 电荷数(绝对值)不相同
电荷数(绝对值)不相同
C.![]() 的熔点比的
的熔点比的![]() 高主要是因为
高主要是因为![]() 的晶格能比
的晶格能比![]() 大
大
D.![]() 晶体固态时也能导电
晶体固态时也能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计以下实验方案,从海带中提取I2。
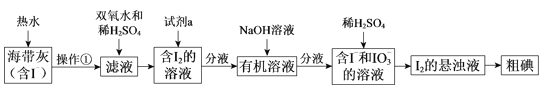
(1)操作①的名称是______。
(2)向滤液中加入双氧水的作用是______。
(3)试剂a可以是______(填序号)。
①四氯化碳 ②苯 ③酒精 ④乙酸
(4)I–和IO3-在酸性条件下生成I2的离子方程式是________________。
(5)上图中,含I2的溶液经3步转化为I2的悬浊液,其目的是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA表示阿伏加德罗常数的值,下列说法正确的是( )
①1mol金属钠加热时完全反应,转移电子数为NA
②标准状况下,22.4L水中分子数为NA
③1L2mo/L的氯化镁溶液中含氯离子数目为4NA
④0.5molFe与足量稀HCl反应时,转移的电子数为2NA
⑤46gNO2和N2O4混合气体中含有原子数为3NA
A. ①③④⑤ B. ③④ C. ①③⑤ D. ①②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家。磷酸铁锂锂离子电池充电时阳极反应式为,![]() ,放电工作示意图如图。下列叙述不正确的是
,放电工作示意图如图。下列叙述不正确的是

A.放电时,Li+通过隔膜移向正极
B.放电时,电子由铝箔沿导线流向铜箔
C.放电时正极反应为:![]()
D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,C、Fe、P元素化合价均不发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
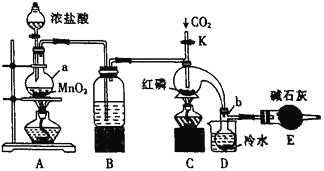
【题目】三氯化磷![]() 是一种重要的有机合成催化剂。实验室常用红磷与干燥的
是一种重要的有机合成催化剂。实验室常用红磷与干燥的![]() 制取
制取![]() ,装置如图所示。
,装置如图所示。
已知:![]() 的熔点为
的熔点为![]() ,沸点为
,沸点为![]() ,易被氧化,遇水易水解,与
,易被氧化,遇水易水解,与![]() 反应生成
反应生成![]() 。
。
请回答下列问题:
(1)装置A中发生反应的化学方程式为___________。
(2)仪器b的名称是___________,装置B中所装试剂名称是___________,装置E中碱石灰的作用是___________。
(3)实验时,检查装置气密性后,向装置C的曲颈瓶中加入红磷,打开止水夹K通入干燥的![]() ,一段时间后,关闭K,加热曲颈瓶至上部有黄色升华物出现时通入氯气,反应立即进行。通入干燥
,一段时间后,关闭K,加热曲颈瓶至上部有黄色升华物出现时通入氯气,反应立即进行。通入干燥![]() 的作用是___________。
的作用是___________。![]() 不能用
不能用![]() 代替,理由是___________。
代替,理由是___________。
(4)装置D的作用是___________。
(5)![]() 水解得到亚磷酸
水解得到亚磷酸![]() ,二元弱酸
,二元弱酸![]() ,写出亚磷酸钠被浓硝酸氧化的离子方程式:___________。
,写出亚磷酸钠被浓硝酸氧化的离子方程式:___________。
(6)经分析,![]() 产品中含有少量
产品中含有少量![]() ,某同学设计如下实验测定
,某同学设计如下实验测定![]() 的纯度:取
的纯度:取![]() 产品于锥形瓶中,加入过量稀硝酸,振荡充分反应,然后加入足量的硝酸银溶液,完全反应后过滤,滤渣经干燥后称量得
产品于锥形瓶中,加入过量稀硝酸,振荡充分反应,然后加入足量的硝酸银溶液,完全反应后过滤,滤渣经干燥后称量得![]() 。则该产品中
。则该产品中![]() 的质量分数为___________
的质量分数为___________![]() 保留两位有效数字
保留两位有效数字![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 2.9 g 的某有机物完全燃烧,生成 6.6 gCO2 和 2.7 gH2O,下列说法正确的是
A.该有机物只含 C、H 两种元素B.该有机物中可能含有氧元素
C.该有机物的分子式是 C3H6OD.该有机物含有 C、H、O 三种元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠被用作肉制品发色剂、防腐剂等,硝酸钠在肉制品加工中作发色剂。但亚硝酸钠是食品添加剂中急性毒性较强的物质之一,是一种剧毒药,摄取少量亚硝酸盐进入血液后,可使正常的血红蛋白变成正铁血红蛋白而失去携带氧的功能,导致组织缺氧。硝酸钠的毒性作用主要是由于它在食物中、在水中或在胃肠道内被还原成亚硝酸盐所致。亚硝酸钠生产方法是由硝酸生产过程中的氮氧化物气体![]() 、
、![]() 用氢氧化钠或碳酸钠溶液吸收制得。硝酸钠的生产方法是将硝酸生产中的尾气用碱液吸收后,经硝酸转化,再用碱中和、蒸发、结晶、分离制得。
用氢氧化钠或碳酸钠溶液吸收制得。硝酸钠的生产方法是将硝酸生产中的尾气用碱液吸收后,经硝酸转化,再用碱中和、蒸发、结晶、分离制得。
![]() 实验室可用加热亚硝酸钠与氯化铵的浓溶液制取氮气,写出该反应的化学方程式:______ ;将亚硝酸钠溶液滴加到含淀粉的酸性KI溶液中,可观察到溶液变蓝色,写出该反应的离子方程式:______ ;将亚硝酸钠溶液滴加到
实验室可用加热亚硝酸钠与氯化铵的浓溶液制取氮气,写出该反应的化学方程式:______ ;将亚硝酸钠溶液滴加到含淀粉的酸性KI溶液中,可观察到溶液变蓝色,写出该反应的离子方程式:______ ;将亚硝酸钠溶液滴加到![]() 酸性溶液中,可观察到溶液的颜色由 ______ 色变为绿色,写出该反应的离子方程式:______ 。
酸性溶液中,可观察到溶液的颜色由 ______ 色变为绿色,写出该反应的离子方程式:______ 。
![]() 写出氮氧化物
写出氮氧化物![]() 、
、![]() 与氢氧化钠溶液反应生成亚硝酸钠溶液的离子方程式:______ ;若用
与氢氧化钠溶液反应生成亚硝酸钠溶液的离子方程式:______ ;若用![]() 溶液吸收
溶液吸收![]() 可生成
可生成![]() ,
,![]() 和
和![]() 溶液完全反应时转移电子
溶液完全反应时转移电子![]() ,则反应的离子方程式为 ______ 。
,则反应的离子方程式为 ______ 。
![]() 从下列试剂中选用部分试剂鉴别亚硝酸钠、硝酸钠和氯化钠三种无色溶液,它们是 ______ 。
从下列试剂中选用部分试剂鉴别亚硝酸钠、硝酸钠和氯化钠三种无色溶液,它们是 ______ 。
A.稀盐酸![]() 溶液
溶液![]() 稀硝酸
稀硝酸![]() 氢氧化钠溶液
氢氧化钠溶液
![]() 等物质的量浓度的亚硝酸钠、氯化钠、碳酸钠三种溶液中阴离子总浓度由大到小的顺序是 ______
等物质的量浓度的亚硝酸钠、氯化钠、碳酸钠三种溶液中阴离子总浓度由大到小的顺序是 ______ ![]() 填溶液中溶质的化学式
填溶液中溶质的化学式![]() 。
。
![]() 工业品硝酸钠含少量杂质
工业品硝酸钠含少量杂质![]() 、
、![]() 、NaCl、水不溶物
、NaCl、水不溶物![]() ,某同学欲测定工业品硝酸钠的纯度,进行了如下实验:
,某同学欲测定工业品硝酸钠的纯度,进行了如下实验:
![]() 称取
称取![]() 干燥工业品硝酸钠,投入盛适量蒸馏水的烧杯中,充分搅拌后加入10mL
干燥工业品硝酸钠,投入盛适量蒸馏水的烧杯中,充分搅拌后加入10mL![]() 的A溶液
的A溶液![]() 足量
足量![]() ,充分反应后过滤;
,充分反应后过滤;
![]() 向滤液中加入足量KI溶液和适量稀硫酸,充分反应后将所得溶液配成1000mL溶液;
向滤液中加入足量KI溶液和适量稀硫酸,充分反应后将所得溶液配成1000mL溶液;
![]() 取
取![]() 所配溶液于锥形瓶中,加入少量B物质,再用
所配溶液于锥形瓶中,加入少量B物质,再用![]() 的
的![]() 溶液滴定,用去
溶液滴定,用去![]() 溶液
溶液![]() 。
。
(有关反应为:![]()
![]() 溶液中的溶质的化学式是 ______ ,加入A溶液的作用是 ______ 。
溶液中的溶质的化学式是 ______ ,加入A溶液的作用是 ______ 。
![]() 物质是 ______ ,滴定终点时的颜色变化是 ______ 。
物质是 ______ ,滴定终点时的颜色变化是 ______ 。
![]() 若该同学操作正确,但结果造成测定结果略偏高,其原因可能是
若该同学操作正确,但结果造成测定结果略偏高,其原因可能是![]() 任写一点
任写一点![]() ______ 。
______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究不同条件对相同体积相同物质的量浓度的 H2O2分解速率的影响,得到如下数据。由此不能得出的结论是:

A. Cu2+与 Fe3+对 H2O2 分解都有催化作用,但 Cu2+催化效果更好
B. 由Ⅰ与Ⅱ可知其它条件相同时,时间越长, H2O2 分解越彻底
C. 由Ⅰ与Ⅲ可知其它条件相同时,温度越高, H2O2 分解越快
D. 由Ⅰ与Ⅲ可知其它条件相同时,碱性越强, H2O2 分解越快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com