
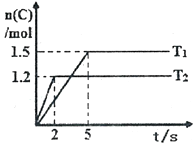
 现将2molA和1molB加入2L密闭容器中发生反应:2A(g)+B(g)?2C(g),分别在Tl和T2时测得生成物C的物质的量随时间变化如图所示,下列说法正确的是( )
现将2molA和1molB加入2L密闭容器中发生反应:2A(g)+B(g)?2C(g),分别在Tl和T2时测得生成物C的物质的量随时间变化如图所示,下列说法正确的是( )| A. | T1<T2 | |
| B. | 该反应在温度为T1时达到平衡时,容器中A与C的物质的量浓度相等 | |
| C. | 温度为T2时,2s内B的平均速率为0.3mol•L-1•s-l | |
| D. | 温度为T1时,达平衡时反应物A的转化率为60% |
分析 A.温度越高,反应速率越快,优先达到平衡状态;
B.温度为T1达到平衡时,C的物质的量为1.5mol,结合反应计算出平衡时A的物质的量;
C.先计算出温度为T2时2s内C的平均速率,然后利用反应速率与化学计量数成正比计算出v(B);
D.温度为T1时,达到平衡时C的物质的量为1.5mol,结合反应方程式计算出消耗A的物质的量,然后计算出A的转化率.
解答 解:A.根据图象可知,温度为T2时优先达到平衡状态,说明温度T2较高,即T1<T2,故A正确;
B.温度为T1达到平衡时,C的物质的量为1.5mol,根据反应2A(g)+B(g)?2C(g)可知平衡时消耗A的物质的量为1.5mol,则平衡时A的物质的量为:2mol-1.5mol=0.5mol,根据c=$\frac{n}{V}$可知A、C的物质的量浓度不相等,故B错误;
C.温度为T2时,2s内A的平均反应速率为:v(C)=$\frac{\frac{1.2mol}{2L}}{2s}$=0.3mol•L-1•s-l,反应速率与化学计量数成正比,则B的平均速率为:v(B)=$\frac{1}{2}$v(C)=0.15mol•L-1•s-l,故C错误;
D.温度为T1达到平衡时,C的物质的量为1.5mol,根据反应2A(g)+B(g)?2C(g)可知平衡时消耗A的物质的量为1.5mol,则A的转化率为:$\frac{1.5mol}{2mol}$×100%=75%,故D错误;
故选A.
点评 本题考查化学平衡的计算,题目难度中等,涉及化学平衡及其影响、化学反应速率计算、转化率计算等知识,明确化学平衡及其影响为解答关键,注意掌握化学反应速率与化学计量数的关系,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
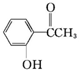 乙:
乙: ,丙:
,丙: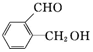
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C=C | C-C | C≡C | C-H |
| E(kJ/mol) | 436 | 615 | 347.7 | 812 | 413.4 |
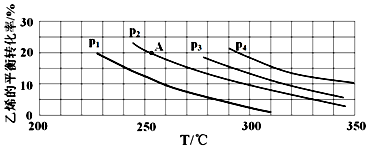
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验 序号 | 时间/min 浓度/mol•L-1 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 950 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 24gNaH中阴离子所含电子总数为2NA | |
| B. | 标准状况下,44.8LNO与22.4LO2混合后,气体中分子总数为2NA | |
| C. | 在0.lmol/L的K2CO3溶液中,阴离子数目大于O.1NA | |
| D. | 300mL2mol/L乙醇溶液中所含分子数为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com