
【化学——物质结构与性质】
A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大。B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族。B、C、D的最高价氧化物的水化物均能互相反应生成盐和水,D的原子半径是同周期原子中最小的。
根据以上信息,回答下列问题:
(1)上述A、B、C、D四种元素中第一电离能最小的是 ,电负性最大的是 , 原子半径由小到大的顺序为 。 (填相关元素的元素符号)
 (2)A和D的氢化物中,沸点较高的是 (填相关物质的分子式);其原因是 。
(2)A和D的氢化物中,沸点较高的是 (填相关物质的分子式);其原因是 。
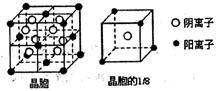
(3)A和E可形成离子化合物,其晶胞结构如右图所示:则每个晶胞中含阳离子的数目为 ,含阴离子的数目为 ,该离子化合物的化学式为 。
科目:高中化学 来源: 题型:
有机物D是一种合成抗高血压药的重要通用中间体,其合成路线如下:(已知A是一种芳香酸)
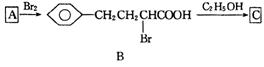
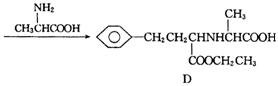
(1)A、C的结构简式分别是 、 ,D中含有的含氧官能团名称是 。
(2)C→D的反应类型是 。
(3)加热条件下,C在足量NaOH水溶液中反应的化学方程式是 。
(4)E是一种相对分子质量比A小14的芳香酸。写出满足下列条件的E的所有同分异构体的结构简式:
。
①能发生银镜反应 ②一定条件下可发生水解反应 ③分子的核磁共振氢谱中有四组峰
(5)F是B在碱溶液中水解后再酸化的产物。F在一定条件下可聚合成高分子化合物,写出该反应的化学方
程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)(2013·浙江理综,8A)实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 ( )
(2)从海水中提取物质都必须通过化学反应才能实现 ( )
(2013·福建理综,6B)
(3)次氯酸钠溶液可用于环境的消毒杀菌 ( )
(2013·四川理综,1D)
(4)在“火柴头中氯元素的检验”实验中,摘下几根未燃过的火柴头,将其浸于水中,稍后取少量溶液于试管中,滴加硝酸银溶液和稀硝酸后,即可判断氯元素的存在( )
(2012·浙江理综,8B)
(5)根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO 溶液中能生成HClO( )
(2011·安徽理综,11D)
(6) ①湿润红纸条;②饱和氯水。①中红纸条褪色 ( )
①湿润红纸条;②饱和氯水。①中红纸条褪色 ( )
(2012·北京理综,10D)
(7) ①酚酞溶液;②浓盐酸。①中无明显变化 ( )
①酚酞溶液;②浓盐酸。①中无明显变化 ( )
(2012·北京理综,10B)
查看答案和解析>>
科目:高中化学 来源: 题型:
氢溴酸在医药和石化工业上有广泛用途。如图所示是模拟工业制备氢溴酸粗产品并精制的流程:
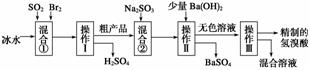
根据上述流程回答下列问题:
(1)混合①中发生反应的离子方程式为_______________________________________。
(2)混合①中使用冰水的目的是____________________________________________。
(3)操作Ⅲ一般适用于分离________混合物(填序号)。
a.固体和液体 b.固体和固体
c.互不相溶的液体 d.互溶的液体
(4)混合②中 加入Na2SO3的目的是__________________________________________。
加入Na2SO3的目的是__________________________________________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色。于是甲乙两同学设计了简单实验进行探究:
甲同学假设工业氢溴酸呈淡黄色是因为其中含有Fe3+,则用于证明该假设所用的试剂为________,若假设成立可观察到的现象为________________;乙同学假设工业氢溴酸呈淡黄色是因为其中含有______________________,其用于证明该假设所用的试剂为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
 25℃时,满足c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的醋酸和醋酸钠混合溶液中,c(CH3COO-)与pH的关系如图所示。下列叙述错误的是
25℃时,满足c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的醋酸和醋酸钠混合溶液中,c(CH3COO-)与pH的关系如图所示。下列叙述错误的是
A.该温度下醋酸的电离常数Ka为l0-4.75mol·L-l
B.M点所表示的溶液中:
c(Na+)+c(H+)+c(CH3COOH)=0.1 mol·L-1
C.N点所表示的溶液中:
c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
D.Q点所表示的溶液中加入等体积的0.05mol·L-1NaOH溶液充分反应后pH>7
查看答案和解析>>
科目:高中化学 来源: 题型:
肾上腺素可用于支气管哮喘过敏性反应,其结构简式如下。下列关于肾上腺
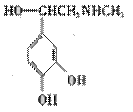 素的叙述正确的是 ( )
素的叙述正确的是 ( )
A.该物质的分子式为C9H16NO3
B.该物质不能发生消去反应
C.1mol该物质与NaOH溶液反应,消耗2molNaOH
D.该物质与浓溴水既能发生取代反应,又能发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬
燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)=CH4(g)+C2H2 (g)+H2(g) △H1=+156.6 kJ·mol-1
C3H6 (g)=CH4(g)+C2H2 (g ) △H2=+32.4 kJ·mol-1
则相同条件下,反应C3H8(g)= C3H6 (g)+H2(g) 的△H = kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙
烷,电解质是熔融碳酸盐。电池负极反应式为 ;放电时CO32-移向电池的 (填“正”或“负”)极。
查看答案和解析>>
科目:高中化学 来源: 题型:
下面四个反应中,反应类型与其它三种不同的是
A.CH3CH2OH + CH3COOH CH3COOCH2CH3 + H2O
B.CH3CH2OH CH2=CH2↑+H2O
CH2=CH2↑+H2O
C.2CH3CH2OH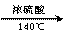 CH3CH2OCH2CH3 + H2O
CH3CH2OCH2CH3 + H2O
D. CH3CH2OH + HBr CH3CH2Br + H2O
CH3CH2Br + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
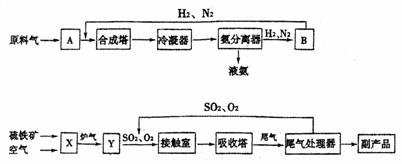
合成氨工业、硫酸工业的生产工艺流程大致为:
合成塔和接触室中的反应分别为:
 |
N2(g)+3H2(g)  2NH3(g) △H﹤0; 2SO2(g)+O2(g)
2NH3(g) △H﹤0; 2SO2(g)+O2(g)  2SO3(g) △H﹤0
2SO3(g) △H﹤0
(1)写出流程中设备的名称:B ,X 。
(2)写出硫铁矿和空气反应的化学方程式
(3)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是 。
(4)采用循环操作可提高原料的利用率,下列生产中,采用循环操作的
是 (填序号)。
①硫酸工业 ②合成氨工业 ③硝酸工业
(5)工业上常用98.3%的浓硫酸吸收SO3而不用稀硫酸或水的原因是 。
(6)工业生产中常用氨——酸法进行尾气脱硫,以达到消除污染、废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com