
| A、23 g钠在氧气中完全燃烧失去电子数为NA |
| B、标准状况下,22.4L已烷所含碳原子数为6NA |
| C、20℃、1.01×105Pa时,1.6gC2H4和1.2g CO的混合气体,含气体分子数为0.1NA |
| D、0.1L 3mol?L-1的Al2(SO4)3溶液中含有的Al3+数目为0.6NA |


科目:高中化学 来源: 题型:
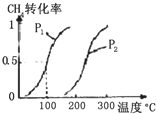 甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,来制备甲醇.
甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,来制备甲醇.| 实验编号 | T(°C) | n(CO)/n(H2) | p(MPa) | ||
| I | 150 |
|
0.1 | ||
| II | 5 | ||||
| III | 350 | 5 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 2 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | NaCl | KCl | NaClO3 | KClO3 | KOH |
| 价格(元/50kg) | 500 | 1900 | 4200 | 26000 | 10600 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用阳离子交换膜法电解饱和食盐水制取烧碱 |
| B、将黏土和石灰石研磨成粉末,再混合均匀即可得普通水泥 |
| C、目前合成氨,没有采用更大压强是从设备和动力要求方面考虑的 |
| D、生产硫酸时,接触室内热交换器的作用是预热进入的炉气和冷却反应生成的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠溶于水中:2Na+2H2O=2Na++2OH-+H2↑ |
| B、足量氯气通入FeCl2溶液中:Cl2+Fe2+=Fe3++2Cl- |
| C、过量氨水加入AlCl3溶液中:Al3++3OH-=Al(OH)3↓ |
| D、实验室用Ca(OH)2和NH4Cl制取氨气:OH-+2NH4+=NH3↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com