
| A. | 四项 | B. | 三项 | C. | 二项 | D. | 一项 |
分析 ①元素化合价的绝对值+该元素原子最外层电子数=8,元素原子满足8电子结构;
②分子晶体的堆积不一定是分子密堆积,如冰晶体中存在氢键,不是分子密堆积;
③NaCl晶胞结构为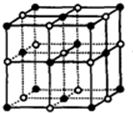 ,晶体中与每个Na+距离相等且最近的Na+个数=3×8÷2;
,晶体中与每个Na+距离相等且最近的Na+个数=3×8÷2;
④稀有气体单质不存在任何化学键;
⑤分子晶体由固体变为气体,克服分子间作用力;
⑥晶体有自范性,而非晶体没有,单晶体各向异性,多晶体则为各向同性;
⑦SiC晶胞与金刚石一样;
⑧中心原子采取sp3杂化的分子,VSEPR模型是正四面体,但其立体构形不一定是正四面体.
解答 解:①NCl3分子中N元素化合价为-3,N原子最外层电子数为5,所以3+5=8,N原子达8电子结构;Cl元素化合价为+1价,F原子最外层电子数为7,1+7=8,Cl原子满足8结构,故①错误;
②分子晶体的堆积不一定是分子密堆积,如冰晶体中存在氢键,不是分子密堆积,故②错误;
③NaCl晶胞结构为 ,NaCl晶体中与每个Na+距离相等且最近的Na+个数=3×8÷2=12,故③正确;
,NaCl晶体中与每个Na+距离相等且最近的Na+个数=3×8÷2=12,故③正确;
④稀有气体单质不存在任何化学键,故④错误;
⑤分子晶体由固体变为气体,克服分子间作用力,C60、I2均为分子晶体,则C60气化和I2升华克服的作用力相同,故⑤正确;
⑥晶体的规则几何外形是自发形成的,有些固体尽管有规则的几何外形,但由于不是自发形成的,所以不属于晶体,所以晶体具有自范性,非晶体没有自范性,但单晶体各向异性,多晶体和非晶体则为各向同性,所以不能用各向异性来区分晶体和非晶体,故⑥错误;
⑦SiC晶胞与金刚石一样,所以1个SiC晶胞中一共有8个原子,故⑦错误;
⑧中心原子采取sp3杂化的分子,VSEPR模型是正四面体,但其立体构形不一定是正四面体,如:水和氨气分子中中心原子采取sp3杂化,但H2O是V型,NH3是三角锥型,故⑧正确;
故选B.
点评 本题考查晶体类型与结构、性质等,难度不大,注意基础知识的掌握与晶体中的特殊性.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH在电池的负极上参加反应 | |
| B. | 在外电路中电子由负极沿导线流向正极 | |
| C. | 1 mol乙醇被氧化转移6 mol电子 | |
| D. | 电池正极得电子的物质是O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在一个基态多电子的原子中,不可能有两个能量完全相同的电子 | |
| B. | 金属Na、Mg、Al的硬度依次降低 | |
| C. | 由原子间通过共价键而形成的晶体一般具有高的熔、沸点及硬度 | |
| D. | PCl3和CO32-的中心原子的杂化方式相同,都是sp3杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
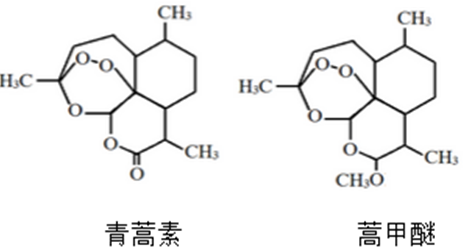
| A. | 蒿甲醚的相对分子质量为295 | |
| B. | 蒿甲醚结构中含有两个酯基 | |
| C. | 二者互为同分异构体 | |
| D. | 二者均既具有氧化性,又具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为某种燃料电池的工作原理示意图,a、b 均为惰性电极.
如图为某种燃料电池的工作原理示意图,a、b 均为惰性电极.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg电极是该电池的正极 | |
| B. | 电池工作时实现了电能向化学能的转化 | |
| C. | H2O2在石墨电极上发生还原反应 | |
| D. | 电子从石墨电极流向Mg电极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com