镍具有优良的物理和化学特性,是高技术产业的重要原料.羰基法提纯粗镍涉及的两步反应依次为:
反应I Ni(s)+4CO(g)
Ni(CO)
4(g)△H
1<0
反应II Ni(CO)
4(g)
Ni(s)+4CO(g)△H
2反应I和反应Ⅱ分别在连通的A装置和B装置中同时进行,A、B容积之和为2L.
(1)在温度不变的情况下,要提高反应I中Ni(CO)
4的产率,可采取的措施有
、
.
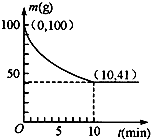
(2)350K时,在装置A中装有100g粗镍(纯度98.5%,所含杂质不与CO反应),通入4mol CO气体制备Ni(CO)
4,装置A中剩余固体质量和反应时间的关系如图所示.
①若10min达到平衡时得到29.5g纯镍,则反应I的平衡常数K
1为
.
②0~10min的平均反应速率υ[Ni(CO)
4]=
.
(3)反应Ⅱ中△H
2
0(填“>”、“<”或“=”);若反应Ⅱ达到平衡后,保持其他条件不变,降低B装置温度,重新达到平衡时
.
a.平衡常数K
2增大 b.CO的浓度减小
c.Ni的质量减小 d.υ逆[Ni(CO)
4]增大
(4)用吸收H
2后的稀土储氢合金作为电池负极材料(用MH表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量,长寿命的镍氢电池.电池充放电时的总反应为:NiO(OH)+MH
Ni(OH)
2+M,电池充电时,阳极的电极反应式为
.电池充电时阴极上发生
(填“氧化”或“还原”)反应.

 镍具有优良的物理和化学特性,是高技术产业的重要原料.羰基法提纯粗镍涉及的两步反应依次为:
镍具有优良的物理和化学特性,是高技术产业的重要原料.羰基法提纯粗镍涉及的两步反应依次为:

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案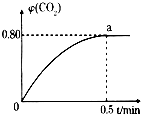 运用化学反应原理研究碳的化合物具有重要意义.
运用化学反应原理研究碳的化合物具有重要意义.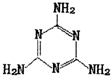 Ⅰ.CN-能与Ni2+形成[Ni(CN)4]2-配离子
Ⅰ.CN-能与Ni2+形成[Ni(CN)4]2-配离子