
| A.①②③ | B.①③ | C.②④ | D.①③⑤ |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:实验题
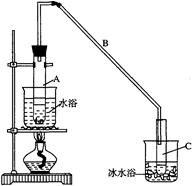

| | 密度 (g/cm3) | 熔点 (℃) | 沸点 (℃) | 溶解性 |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
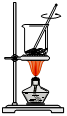 |  |  |  |
| A.海带灼烧成灰 B.过滤得含I-溶液 C.放出碘的苯溶液 D.分离碘并回收苯 | |||
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
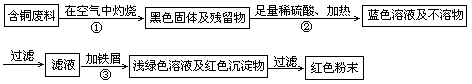
 2CuSO4+2H2O ) ,于是他提出了另一套方案:
2CuSO4+2H2O ) ,于是他提出了另一套方案: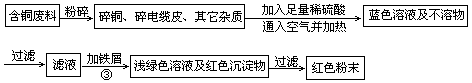
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硫酸钠、硫化钠、亚硫酸钾、硫代硫酸钾、偏铝酸钠 |
| B.氯化铁、氯化铵、硫酸钠、硫酸镁、硫酸铝 |
| C.硫氰化钾、氯化钾、苯酚、硫酸钠、碳酸钠 |
| D.氯化铝、盐酸、氯化钠、氯化钡、氢氧化钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com