
下列反应,其反应生成物的颜色按红、红褐、淡黄、蓝色顺序排列的是( )
①金属钠在纯氧中燃烧 ②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间 ③FeCl3溶液中滴入KSCN溶液 ④无水硫酸铜放入医用酒精中
A.②③①④ B.③②①④
C.③①②④ D.①②③④
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
某化学小组用如图所示装置制取氯气。下列说法不正确的是( )
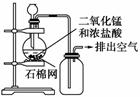
A.该装置图中至少存在三处明显错误
B.该实验中收集氯气的方法不正确
C.为了防止氯气污染空气,必须进行尾气处理
D.在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸可以证明是否有氯气逸出
查看答案和解析>>
科目:高中化学 来源: 题型:
酸雨是指天空降水呈酸性(pH小于5.6),个别地方酸雨的pH竟低于2.1(食醋的pH=3)。形成酸雨的主要是大气中的SO2和氮氧化物。它们的主要来源是煤和石油的燃烧,全世界每年有1.5亿吨SO2的排放量。
(1)SO2可在空气中受光照被氧化,最终与雨水形成酸雨。试写出这两个化学反应方程式:
________________________________________________________________________
________________________________________________________________________。
(2)汽车排放的尾气、硝酸厂和化肥厂的废气都含氮氧化物,全世界每年排放量约5×107 kg。NO2溶于水生成________酸。
(3)酸雨可导致的危害有( )
A.腐蚀建筑物 B.导致树木枯萎
C.造成洪涝灾害 D.恶化人类环境
(4)为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫化物进行________,对废气中的氮氧化物进行________。
查看答案和解析>>
科目:高中化学 来源: 题型:
制印刷电路板时常用FeCl3溶液作为“腐蚀液”,发生的反应为2FeCl3+Cu===2FeCl2+CuCl2,向盛有FeCl3溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是( )
A.烧杯中有铜无铁 B.烧杯中有铁无铜
C.烧杯中铁、铜都有 D.烧杯中铁、铜都无
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列物质中所含的杂质(括号内为杂质),将选用的试剂和分离方法填在题后的横线上,并写出有关反应的离子方程式。
(1)Fe2O3[Fe(OH)3]______________________________;
(2)Fe2O3(Al2O3)_________________________________________________________;
(3)FeCl3(FeCl2)__________________________________________________________;
(4)FeCl2(FeCl3)___________________________________________________________;
(5)FeCl2(CuCl2)___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应N2+3H2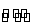 2NH3的能量变化如图所示,该反应的热化学方程式是
2NH3的能量变化如图所示,该反应的热化学方程式是
( )

A.N2(g)+3H2(g)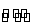 2NH3(l) ΔH=2(a-b-c) kJ·mol-1
2NH3(l) ΔH=2(a-b-c) kJ·mol-1
B.N2(g)+3H2(g)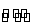 2NH3(g) ΔH=2(b-a) kJ·mol-1
2NH3(g) ΔH=2(b-a) kJ·mol-1
C.1/2N2(g)+3/2H2(g)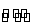 NH3(l) ΔH=(b+c-a) kJ·mol-1
NH3(l) ΔH=(b+c-a) kJ·mol-1
D.1/2N2(g)+3/2H2(g)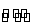 NH3(g) ΔH=(a+b) kJ·mol-1
NH3(g) ΔH=(a+b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数。下列叙述正确的是 ( )
A.1mol甲醇中含有C-H键的数目为4NA
B.标准状况下,2.24L已烷含有分子的数目为0.1NA
C.12克金刚石中含有的共价键数目为2NA
D.1 mol 甲基所含的电子数为10NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com