
下列说法正确的是
A.根据溶液中有CH3COOH、CH3COO-和H+即可证明CH3COOH达到电离平衡状态
B.根据溶液中CH3COO-和H+的物质的量浓度相等即可证明CH3COOH达到电离平衡状态
C.当NH3·H2O达到 电离平衡时,溶液中NH3·H2O、NH4+和OH-的浓度相等
电离平衡时,溶液中NH3·H2O、NH4+和OH-的浓度相等
D.H2CO3是分步电离的,电离程度依次减弱
科目:高中化学 来源:2016-2017学年天津市河东区高二上学期期中质检化学试卷(解析版) 题型:实验题
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。

回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由 。
(5)用相同浓度和体积的稀醋酸代替稀盐酸进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古高三上学期期中化学试卷(解析版) 题型:填空题
已知在常温常压下:
①2C H3OH(l)+3O2(g)=2CO2(g)+4
H3OH(l)+3O2(g)=2CO2(g)+4 H2O(l) ΔH=-1451.6kJ/mol
H2O(l) ΔH=-1451.6kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ/mol
(1)写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式_______________
(2)某小组根据甲醇燃烧的反应原理,设计如图所示的电池装置:
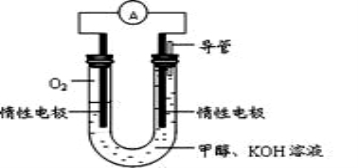
该电池正极的电极反应式____________________
工作一段时间后,测得溶液的pH______________(填增大、减小或不变),则该电池总反应的离子方程式__________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:填空题
电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
化学式 | 电离平衡常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为_____________________。
(2)25 ℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)________c(CH3COO-)(填“>”、“<”或“=”)。
(3)NaCN溶液中通入少量CO2,所发生反应的化学方程式为___________________。
(4)25 ℃时, pH=8的CH3COONa溶液中,c(Na+)- c(CH3COO-)=_________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:选择题
常温下有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和Na2SO4溶液中的一种。已知A、B溶液中水的电离程度相同,A、C溶液的pH相同。下列说法中不正确的是
A.D溶液的pH=7
B.四种溶液相比,C溶液中水的电离程度最大
C.A与C等体积混合后,溶液中有c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.B与D等体积混合后,溶液中有c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:选择题
某学生欲完成反应2HCl+2Ag=2AgCl+H2↑而设计了下列四个实验,你认为可行的是
A.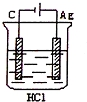 B.
B. C.
C.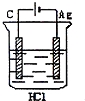 D.
D.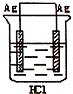
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:选择题
下列说法正确的是
A.任何酸与碱发生中和反应生成1molH2O的过程中,能量变化均相同
B.中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
C.若①2H2(g)+O2(g)=2H2O(g)△H=-akJ·mol-1,
②2H2(g)+O2(g)=2H2O(l)△H=-bkJ·mol-1,则a>b
D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:选择题
下列各组热化学方程式中,化学反应的△H前者大于后者的是( )
①C(s)+O2(g)=CO2(g)△H1;C(s)+1/2O2(g)=CO(g)△H2
②S(s)+O2(g)=SO2(g)△H3;S(g)+O2(g)=SO2(g)△H4
③H2(g)+1/2O2(g)=H2O(l)△H5;2H2(g)+O2(g)=2H2O(l)△H6
④CaCO3(s))=CO2(g)+CaO(s)△H7;CaO(s)+H2O(l)=Ca(OH)2(s)△H8
A.①③ B.④ C.②③④ D.②③
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:实验题
为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。实验装置如图所示:(固定装置已略去)

(1)A中反应的化学方程式为 。
(2)F烧杯中的溶液通常是  。
。
(3)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是 。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是 。
(5)为说明浓硫酸中的水是否影响B装置现象的判断,还须进行一次实验。实验方案为 。
(6)将57.6g的Cu片加入50mL 18 mol/L的H2SO4溶液中并加热,被还原的H2SO4的物质的量为_________
A.小于0.45 mol
B.等于0.45 mol
C.在0.45 mol和0.90 mol之间
D.等于0.90 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com