
下列解释实际应用的原理表达式中,不正确的是
A. 用排饱和食盐水法收集 :
:


B. 热的纯碱溶液碱性增强:


C. 向 悬浊液中加入
悬浊液中加入 溶液:
溶液: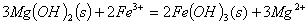
D. 配制FeCl3溶液时为防止溶液浑浊常加入少量稀盐酸Fe3++3H2O Fe(OH)3+3H+,
Fe(OH)3+3H+,
【答案】B
【解析】
试题分析:A. 用排饱和食盐水法收集Cl2,是因为在水中存在可逆反应,Cl2+H2O H++Cl-+HClO,当水中存在Cl-平衡逆向移动,可以减少Cl2的溶解,因此可以用排饱和食盐水的方法收集,正确;B.Na2CO3是强碱弱酸盐水解使溶液显碱性,而盐水解的反应是吸热反应,所以升高温度,盐水解程度增大,溶液的碱性增强,但是盐水解是逐步进行的,因此该表达式错误;C.在Mg(OH)2的悬浊液中存在沉淀溶解平衡,当向该悬浊液中加 入FeCl3溶液时,由于在溶液中c(Fe3+)c3(OH-)>Ksp(Fe(OH)3),所以会形成氢氧化铁沉淀,会发生沉淀转化,正确; D. 配制FeCl3溶液时由于Fe3+水解产生氢氧化铁而使溶液浑浊,所以为抑制水解,防止溶液浑浊常加入少量稀盐酸,正确。
H++Cl-+HClO,当水中存在Cl-平衡逆向移动,可以减少Cl2的溶解,因此可以用排饱和食盐水的方法收集,正确;B.Na2CO3是强碱弱酸盐水解使溶液显碱性,而盐水解的反应是吸热反应,所以升高温度,盐水解程度增大,溶液的碱性增强,但是盐水解是逐步进行的,因此该表达式错误;C.在Mg(OH)2的悬浊液中存在沉淀溶解平衡,当向该悬浊液中加 入FeCl3溶液时,由于在溶液中c(Fe3+)c3(OH-)>Ksp(Fe(OH)3),所以会形成氢氧化铁沉淀,会发生沉淀转化,正确; D. 配制FeCl3溶液时由于Fe3+水解产生氢氧化铁而使溶液浑浊,所以为抑制水解,防止溶液浑浊常加入少量稀盐酸,正确。
考点:考查平衡原理的应用的知识。


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案科目:高中化学 来源: 题型:
I2在KI溶液中存在平衡:  ,某I2、、KI混合溶液中, c(
,某I2、、KI混合溶液中, c( )与温度T的平衡曲线图如下。下列说法不正确的是
)与温度T的平衡曲线图如下。下列说法不正确的是

A. 反应 的△H>0
的△H>0
B.若温度为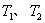 ,反应的平衡常数分别为
,反应的平衡常数分别为
C.若反应进行到状态D时,一定有
D.状态A与状态B相比,状态A的c(I2) 小
查看答案和解析>>
科目:高中化学 来源: 题型:
化学实验室使用的耐高温的石英坩埚的主要成分是________;盛放NaOH溶液的试剂瓶不用玻璃塞而用橡皮塞的原因是________;实验室________(填“能”或“不能”)用玻璃瓶保存氢氟酸,说明原因________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.某温度时, 1LpH=6的水溶液,含 离子
离子
B.含10.6gNa2CO3溶液中,所含阴离子总数等于
C.VLamol/LFeCl3溶液中,若Fe3+离子数目为1mol,则Cl-离子数目大于3mol。
D.电解精炼粗铜时,每转移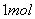 电子,阳极上溶解的
电子,阳极上溶解的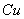 原子数必为
原子数必为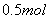
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是
A.用惰性电极电解 溶液分别得到单质
溶液分别得到单质 和Cl2
和Cl2
B.常温下,某溶液中由水电离出的 ,该溶液一定呈酸性
,该溶液一定呈酸性
C. 溶液和
溶液和 溶液加热蒸干、灼烧都得到
溶液加热蒸干、灼烧都得到
D.在AgBr饱和溶液中加入AgNO3溶液,达到平衡时,溶液中Br-浓度降低
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学模拟工业“折点加氯法”处理氨氮废水的原理,进行如下研究。
| 装置(气密性良好,试剂已添加) | 操作 | 现象 |
|
| 打开分液漏斗活塞,逐滴加入浓氨水 | ⅰ.C中气体颜色变浅 ⅱ.稍后,C中出现白烟并逐渐增多 |
(1)浓氨水分解可以制氨气,写出A中反应的化学方程式是 。从平衡移动 的角度分析NaOH固体在氨水分解中的作用 。
(2)现象ⅰ,C中发生的反应为:2NH3(g)+3Cl2(g)= N2(g)+6HCl(g) H= —456 kJ·mol-1
已知:
①NH3的电子式是 。
②断开1mol H-N键与断开1molH-Cl键所需能量相差约为 ,
(3)现象ⅱ中产生白烟的化学方程式是 。
(4)为避免生成白烟,该学生设计了下图装置以完成Cl2和NH3的反应。
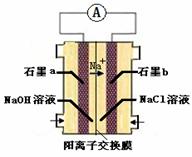
若该装置能实现设计目标,则①石墨b电极上发生的是 反应(填“氧化”或“还原”)
②写出石墨a电极的电极反应式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
检验某晶体是否是铵盐时,将待检物取出少量放在试管中,接下来的操作是 ( )
A.加烧碱溶液,加热,用湿润的红色石蕊试纸放在管口检验
B.直接加热,用湿润的红色石蕊试纸放在管口检验
C.加烧碱溶液,加热,向试管中滴加紫色石蕊试液
D.加水溶解,滴加无色酚酞试液,看是否变红
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式:2SO2(g)+O2(g)2SO3(g) ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是 ( )。
A.相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)
所具有的能量
B.将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为
Q kJ
C.增大压强或升高温度,该反应过程放出更多的热量
D.如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热Q kJ,则此过程中有2 mol SO2(g)被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com