
【题目】托盘天平、容量瓶、量筒是常见的中学化学计量仪器,熟知这些仪器的使用是定量研究化学的基础。
(1)其中标示着使用温度的仪器是________。
(2)下列操作中,容量瓶所具备的功能有________ (填序号)。
A.配制一定体积准确浓度的标准溶液 B.贮存溶液
C.测量容量瓶规格以下的任意体积的溶液 D.准确稀释某一浓度的溶液
E.量取一定体积的液体 F.用来加热溶解固体溶质
(3)如图是某些仪器的刻度部分示意图,图中各仪器虚线为所示读数。其中为量筒的是________(填编号)。读数为________mL。

(4)实验室用98%的浓硫酸配制(浓硫酸密度为1.84g/mL) 450mL 0.1mol/L的硫酸。回答下列问题。
①配制中应选用_______(写出规格) 的容量瓶应量取_____mL 98%的浓硫酸。
②量筒在使用前已洗干净但不干燥,对结果是否造成影响_______(填“是”或“否”),某同学认为将量筒内的浓硫酸倒出之后,应将量筒洗涤一下并将洗涤液并入烧杯中,最后转移到容量瓶中,你认为他的做法_______(填“对“或“错”)。
【答案】 容量瓶、量筒 AD ② 2.5(或2.6) 500mL 2.7 是 错
【解析】试题分析:本题考查化学仪器的使用,物质的量浓度溶液的配制。
(1)托盘天平、容量瓶、量筒三种仪器中标示使用温度的是容量瓶、量筒。
(2)A项,容量瓶用于配制一定体积准确浓度的标准溶液,正确;B项,容量瓶不能贮存溶液,错误;C项,容量瓶上有容量和唯一刻度线,不能测量容量瓶规格以下的任意体积的溶液,错误;D项,容量瓶可准确稀释某一浓度的溶液,正确;E项,容量瓶不能量取一定体积的液体,错误;F项,容量瓶上有温度,容量瓶不能用来加热溶解固体溶质,错误;答案选AD。
(3)根据仪器的特点知:①0刻度在中间,为温度计;②没有0刻度,从下至上数据增大,为量筒;③0刻度在上,为滴定管。量筒的读数为2.5mL。
(4)①配制450mL溶液应选用500mL容量瓶。1.84g/mLV(浓硫酸)![]() 98%=0.1mol/L
98%=0.1mol/L![]() 0.5L
0.5L![]() 98g/mol,V(浓硫酸)=2.7mL。
98g/mol,V(浓硫酸)=2.7mL。
②量筒在使用前已洗干净但不干燥,使得量取的硫酸物质的量偏小,所配溶液浓度偏小,对结果有影响。某同学认为将量筒内的浓硫酸倒出之后,应将量筒洗涤一下并将洗涤液并入烧杯中,最后转移到容量瓶中,他的做法错,若这样做,将使硫酸物质的量偏大,所配溶液浓度偏大。


科目:高中化学 来源: 题型:
【题目】已知:2Zn(s)+O2(g)![]() 2ZnO(s) ΔH=701.0 kJ·mol1
2ZnO(s) ΔH=701.0 kJ·mol1
2Hg(l)+O2(g)![]() 2HgO(s) ΔH=181.6 kJ·mol1
2HgO(s) ΔH=181.6 kJ·mol1
则反应Zn(s)+HgO(s)![]() ZnO(s)+Hg(l)的ΔH为
ZnO(s)+Hg(l)的ΔH为
A.+519.4 kJ·mol1 B.+259.7 kJ·mol1 C.259.7 kJ·mol1 D.519.4 kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84消毒液”能有效杀灭甲型H1N1等病毒,某同学购买了一瓶“威露士”牌“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:“84消毒液”:含25%NaClO、1 000 mL、密度1.19 g·cm-3,稀释100倍(体积比)后使用。同学参阅“威露士”牌“84消毒液”的配方,欲用NaClO固体配制480 mL含25% NaClO的消毒液。下列说法正确的是 ( )
A. 配制时需要的玻璃仪器除烧杯、量筒、容量瓶外还需一种玻璃仪器
B. 容量瓶用蒸馏水洗净后,应烘干才能用于溶液的配制
C. 定容时水加多了应该用滤纸吸出。
D. 需要称量的NaClO固体质量为149 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F为元素周期表中前四周期且原子序数依次增大的六种元素.其中A、B、C、D核电荷数之和为36,A、C原子的最外层电子数之和等于B原子 的次外层电子数,D原子质子数为B原子质子数的两倍,E元素所在主族均为金属,F的价电子数与C的核电荷数相等。
(1)下列关于上述几种元素的说法正确的是_________。
a.B、C、D的原子半径由大到小的顺序为:D >C >B
b.E、F的最外层电子数相等
c.A、B、C、D四种元素中电负性和第一电离能最大的均为B
d.B与C形成的化合物中可能含有非极性键
e.A、C、F都位于周期表的3区
(2)B单质有两种同素异形体.其中在水中溶解度较大的是_______(填化学式)。
(3)EA2和A2B熔点较高的是 _______(填化学式),原因是_________。
(4)D与B可以形成两种分子,其中DB2分子中心原子的杂化类型是____。下列分子或离子中与DB3结构相似的是____________。
a. NH3 b. SO32- c.NO3- d.PCl3
(5)已知B、F能形成两种化合物,其晶胞如下图所示.则高温时甲易转化为乙的原因为 ___________。若乙晶体密度为pg/cm3,则乙晶胞的晶胞边长a =________nm(用含P和NA的式子表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂对工业污泥中的Cr元素回收与再利用的工艺如下(己知硫酸浸取液中的金属离子主要是Cr3+,其次是少量的Fe2+、Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Fe3* | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时 的pH | 1.9 | 7.0 | — | 一 | — |
沉淀完全时 的pH | 3.2 | 9.0 | 11.1 | 8 | 9 (>9溶解) |
(1)实验室用98% (密度为1.84 g·cm-3)的浓硫酸配制200mL4.8 mol·L-1的硫酸溶液,配制时需要量取98%的浓硫酸的体积为_________mL (保留小数点后一位小数),所用的玻璃仪器除烧杯、玻璃棒、量筒外,还需__________________________________。
(2)在上述配制稀硫酸过程中,会导致所配溶液浓度偏小的操作是____________________(填序号)
a.定容时俯视刻度线 b.量取浓硫酸时,俯视刻度线
c.当容置瓶中液体占容积2/3左右时,未振荡摇匀 d.转移溶液时,没有等溶液冷却至室温
(3)加入H2O2的作用一方面是氧化+3价Cr使之转变成+6价Cr (CrO42-或Cr2O72-),以便于与杂质离子分离;另一方面是_____________________________。(离子方程式表示)
(4)调节溶液的pH=8除去的杂质离子是___________________。
(5)钠离子交换树脂的原理为:Mn++nNaR→MRn +nNa+,被交换的杂质离子是_____________________。
(6)通SO2气体时,还原过程发生以下反应(填写缺项物质并配平)
____________________________________________________________Na2SO4.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某样品中含有碳酸钠及少量的硫酸钠和氯化钠,某学生为检验其中的阴离子,按照下图程序进行实验,所加试剂均过量。(可供选择的试剂有:稀硫酸、稀盐酸、稀硝酸、BaCl2溶液、Ba(NO3)2溶液、AgNO3溶液)

回答下列问题:
(1)①试剂1是________结论1是________;
②试剂2是________结论2是________;
③试剂3是________结论3是________ 。
(2)写出有关反应的离子方程式
①__________________;
②__________________;
③__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+、和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过比较分析,认为无须检验就可判断其中必有的两种物质是_______和____________。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当 C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体,则X为__________(填序号)。
a.Br- b. SO42- c.CH3COO- d. HCO3-
(3)将19.2gCu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式_____________________________,若要将Cu完全溶解,至少加入H2SO4的物质的量是___________________________。
(4)E溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态不饱和链烃CnHm在一定条件下与H2加成为CnHm+x,取CnHm和H2混合气体共60mL进行实验,发现随混合气中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温同压下测定).由此可知x的数值为
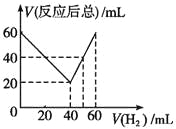
A. 4 B. 3 C. 2 D. 1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关碱金属的说法不正确的是( )
A. 均为IA族元素,最外层均有1个电子
B. 单质的还原性:Li>Na>K>Rb>Cs
C. 碱性:LiOH<NaOH<KOH<RbOH<CsOH
D. 由Li到Cs,核电荷数依次增加,电子层数、原子半径依次增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com