
| 1 |
| 6 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
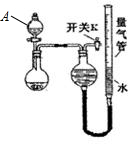
| 编号 | 粉末质量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 2.0g | 10.0mL | 346.2mL |
| ② | 2.0g | 10.0mL | 335.0mL |
| ③ | 2.0g | 10.0mL | 345.8mL |

查看答案和解析>>
科目:高中化学 来源: 题型:
 利用图装置进行下列实验,能得出相应实验结论的是( )
利用图装置进行下列实验,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 |
| A | 浓盐酸 | MnO2 | NaOH溶液 | 制氯气并吸收尾气 |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、 氧化性 |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可以生成白色沉淀 |
| D | 浓硝酸 | Na2CO3 | Na2SiO3 溶液 | 酸性:硝酸>碳酸 >硅酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.8mol?L-1 |
| B、1.0mol?L-1 |
| C、1.2mol?L-1 |
| D、2.0mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 进入2013年以来,我国中东部地区多次遭遇大范围、长时间的雾霾天气.车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.
进入2013年以来,我国中东部地区多次遭遇大范围、长时间的雾霾天气.车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.物质 T/℃n/mol | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.10 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO、NO、NaH、N2 |
| B、SO2、NO2+、N3-、CNO- |
| C、CO32-、NO3-、BeCl2 |
| D、SiF4、SiO44-、SO42-、PO43- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(A)=0.5mol?(L?s)-1 |
| B、v(B)=0.5mol?(L?s)-1 |
| C、v(C)=0.8mol?(L?s)-1 |
| D、v(D)=1mol?(L?s)-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com